Хлори́д ба́рия (хлoристый барий, в просторечии — барий солянокислый, химическая формула — BaCl2) — бинарное неорганическое вещество, относящееся к классу солей.
| Хлорид бария | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Хлорид бария |
| Традиционные названия | Хлористый барий, барий солянокислый |
| Хим. формула | BaCl2 |
| Рац. формула | BaCl2 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 208,246 г/моль |
| Плотность | 3,92 (20 °C) |
| Термические свойства | |
| Температура | |
| • плавления | 962 °C |
| • кипения | 1560 °C |
| Энтальпия | |
| • образования | -860,1 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | 36,2 (20 °C)[1] |
| Классификация | |
| Рег. номер CAS | 10361-37-2 |
| PubChem | 25204, 5360350 и 139046011 |
| Рег. номер EINECS | 233-788-1 |
| SMILES | |
| InChI | |
| RTECS | CQ8750000 |
| ChEBI | 63317 |
| Номер ООН | 1564 |
| ChemSpider | 23540 |
| Безопасность | |
| Предельная концентрация | 0,5 мг/м3 (в воздухе рабочей зоны)[2] |
| ЛД50 | 50-149,2 мг/кг (крысы, орально) |
| Токсичность | Класс опасности 2 |
| Пиктограммы ECB |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Хлорид бария представляет собой бесцветные кристаллы, хорошо растворимые в воде. Ядовит.
Описание
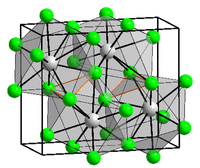
правитьХлорид бария при стандартных условиях представляет собой бесцветные ромбические кристаллы. Малорастворим в спирте, не растворим в диэтиловом эфире, но хорошо растворим в воде. Из водных растворов кристаллизуется дигидрат хлорида бария — бесцветные кристаллы с моноклинной решёткой. ПДК 0,5 мг/м³[2] в воздухе рабочих помещений (в соответствии с ГОСТ 12.1.005-76).
Стандартизация
правитьВ РФ действует ГОСТ 4108-72 «Реактивы. Барий хлорид 2-водный. Технические условия.»
Получение
править1. Взаимодействие металлического бария с хлором:
2. Взаимодействие оксида бария с соляной кислотой:
3. Взаимодействие гидроксида бария с соляной кислотой (реакция нейтрализации):
4. Взаимодействие сульфида бария с хлоридом кальция:
5. Взаимодействие карбоната бария с соляной кислотой:
Химические свойства
править1. Взаимодействие с растворами солей (реакция идёт, если образуется нерастворимое вещество):
2. Взаимодействие с некоторыми кислотами (реакция идёт, если образуется нерастворимое вещество):
3. С парами воды при высокой температуре образует оксид бария[3]:
Сферы применения
правитьХлорид бария применяют в производстве пигментов (например, баритового жёлтого , касселевой зелени и других соединений), в качестве добавки в электролиты при получении магния, для закалки быстрорежущей стали (в виде расплавов смеси хлорида бария с хлоридами щелочных и щёлочноземельных металлов), как компонент керамики, реактив на (сульфат-ион), для утяжеления и осветления кожи в кожевенной промышленности, как зооцид[2].
Имелись также данные, что хлорид бария использовался в медицине, несмотря на ядовитость ионов бария для живых организмов.
Особенности обращения, биологическое действие
правитьВещество токсично. ПДК 0,7 мг/л. При попадании на кожу и в глаза в большом количестве хлористый барий может вызывать химические ожоги; пожаро- и взрывобезопасен.
В связи с возможной токсичностью ионов бария его попадание внутрь организма, насколько это известно, считается недопустимым.
Средняя смертельная доза (ЛД50) для крыс при оральном введении составляет 50-149,2 мг/кг.
II класс опасности по ГОСТ 12.1.007-76.
См. также
правитьПримечания
правитьЛитература
править- Лидин Р. А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист |
