Синдром Вольфа-Паркинсона-Уайта (WPW-синдром) — врождённая аномалия строения сердца. Впервые описана в 1930 году Луисом Вольфом, Джоном Паркинсоном и Полом Дадли Уайтом, а в 1940 году термин «синдром Вольфа-Паркинсона-Уайта» был введён в употребление для обозначения случая наличия у пациента как асистолии, так и пароксизмов тахикардии[3].
| Синдром Вольфа-Паркинсона-Уайта | |
|---|---|
 | |
| МКБ-11 | BC81.4 |
| МКБ-10 | I45.6 |
| МКБ-10-КМ | I45.6 |
| МКБ-9 | 426.7 |
| МКБ-9-КМ | 426.7[1][2] |
| OMIM | 194200 |
| DiseasesDB | 14186 |
| MedlinePlus | 000151 |
| eMedicine | emerg/644 med/2417 |
| MeSH | D014927 |
Общие сведения
правитьСиндром Вольфа-Паркинсона-Уайта — наиболее частый синдром преждевременного возбуждения желудочков (его наблюдают у 0,1 — 0,3 % населения в общей популяции [4][5]), возникающий при наличии дополнительного пучка Кента. Большинство людей при этом не имеют признаков заболевания сердца. У мужчин синдром обнаруживают чаще, чем у женщин.
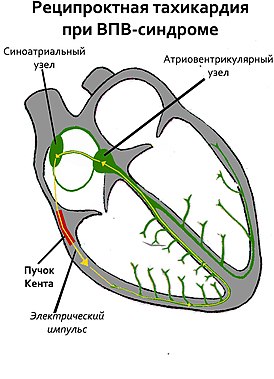
Пучок Кента — аномальный пучок между левым/правым предсердиями и одним из желудочков.[источник не указан 3870 дней] Этот пучок играет важную роль в патогенезе синдрома WPW. Более быстрое распространение импульса через этот дополнительный проводящий путь приводит к:
- 1) укорочению интервала P — R (P — Q);
- 2) более раннему возбуждению части желудочков — возникает Дельта-волна.
Биохимической подоплёкой синдрома является мутации в CBS домене γ2 субъединицы АМФ-активируемой протеинкиназы (AMPK, AMP-activated protein kinase). Консервативный (от прокариотов до человека ) CBS-домен (~ 60 аминокислот) является участком аллостерической регуляции со стороны AMP/ATP.[6]
Этиология
правитьНесмотря на большой прогресс в изучении болезни, молекулярные и генетические основы, ответственные за синдром у большинства пациентов, остаются неизвестными. На март 2020 года известно лишь о нескольких генах, нарушения в которых приводит к синдрому Вольфа — Паркинсона — Уайта[7].
Клиническая картина
правитьУ части больных может не выявляться клинических проявлений. Основное проявление синдрома Вольфа — Паркинсона — Уайта — аритмии. Более чем в 50 % случаев возникают пароксизмальные тахиаритмии: наджелудочковые реципрокные, фибрилляция предсердий, трепетание предсердий. Довольно часто синдром возникает при заболеваниях сердца — аномалии Эбштайна, гипертрофической кардиомиопатии, пролапсе митрального клапана.
Диагностика
правитьСиндром WPW может протекать скрыто (скрытый синдром обычно диагностируют с помощью электрофизиологического исследования). Это связано с неспособностью дополнительных проводящих путей проводить импульсы в антеградном направлении. На ЭКГ во время синусового ритма признаков преждевременного возбуждения желудочков нет. Скрытый синдром WPW проявляется тахиаритмией, его выявление возможно при электростимуляции желудочков.
Явный синдром имеет ряд типичных ЭКГ-признаков:
- Короткий интервал P — R (P — Q) — менее 0,12 с.
- Волна Δ. Её появление связано со «сливным» сокращением желудочков (возбуждение желудочков сначала через дополнительный проводящий путь, а затем через AB-соединение). При быстром проведении через AB-соединение волна Δ имеет больший размер. При наличии AB-блокады желудочковый комплекс полностью состоит из волны Δ, так как возбуждение на желудочки передается только через дополнительный путь.
- Расширение комплекса QRS более 0,1 с за счет волны Δ.
- Тахиаритмии: ортодромная и антидромная наджелудочковые тахикардии, фибрилляция и трепетание предсердий. Тахиаритмии возникают обычно после наджелудочковой экстрасистолы.
Иногда на ЭКГ фиксируется переходящий синдром WPW. Это говорит о том, что попеременно функционируют оба пути проведения импульса — нормальный (АВ-путь) и дополнительный (пучок Кента). В таком случае видны то нормальные комплексы, то деформированные.
Лечение
правитьПрофилактика и лечение пароксизмов тахиаритмии
- Для предупреждения приступов тахикардии при синдроме WPW можно использовать соталол, дизопирамид. Следует помнить, что ряд антиаритмических лекарственных средств может увеличивать рефрактерный период AB-соединения и улучшать проведение импульсов через дополнительные проводящие пути (блокаторы медленных кальциевых каналов, β-адреноблокаторы, сердечные гликозиды), в связи с чем их применение при синдроме WPW противопоказано.
- При возникновении на фоне синдрома фибрилляции предсердий необходимо срочно провести электрическую дефибрилляцию. В последующем рекомендуют провести деструкцию (радиочастотную катетерную аблацию) дополнительных проводящих путей.
Показания для хирургического лечения синдрома Вольфа-Паркинсона-Уайта
- Наличие частых приступов фибрилляции предсердий.
- Приступы тахиаритмии с гемодинамическими нарушениями (коллапс).
- Сохранение приступов тахиаритмии при проведении антиаритмической терапии.
- Ситуации, когда длительная лекарственная терапия нежелательна (молодой возраст, планируемая беременность).
Внутрисердечная радиочастотная абляция — самый эффективный (в 98 % случаев) радикальный способ лечения синдрома WPW. Однако несколько исследований говорят о том, что несмотря на применение этого способа лечения, риск фибрилляции предсердий остаётся высоким по сравнению с населением в целом[7].
Течение и прогноз
правитьДостоверность этого раздела статьи поставлена под сомнение. |
Синдром WPW может быть обнаружен в любом возрасте, даже у новорожденных. Любое сопутствующее заболевание сердца, протекающее с нарушением АВ-проводимости, может способствовать его проявлению. Постоянный синдром WPW, особенно с приступами аритмии, нарушает внутрисердечную гемодинамику, что ведет к расширению камер сердца и снижению сократительной способности миокарда.
Течение заболевания зависит от наличия, частоты и длительности существования тахиаритмий. Внезапная сердечная смерть при синдроме WPW наступает обычно вследствие фатальных аритмий (фибрилляция предсердий, трепетание предсердий, желудочковая тахикардия, фибрилляция желудочков).
Смертность
правитьВнезапная сердечная смерть от синдрома Вольфа — Паркинсона — Уайта наступает примерно у 0.25 — 0.39 % больных ежегодно[7].
Примечания
править- ↑ Disease Ontology (англ.) — 2016.
- ↑ Monarch Disease Ontology release 2018-06-29 — 2018-06-29 — 2018.
- ↑ Ehtisham J., Watkins H. Is Wolff‐Parkinson‐White Syndrome a Genetic Disease? //Journal of cardiovascular electrophysiology. – 2005. – Т. 16. – №. 11. – С. 1258-1262.
- ↑ Genetics Home Reference. Wolff-Parkinson-White syndrome (англ.). Genetics Home Reference. Дата обращения: 24 сентября 2019. Архивировано 27 апреля 2017 года.
- ↑ 1 Внутренние болезни: в 2 т./под ред. А. И. Мартынова. М.: ГЭОТАР — Медиа, 2006. Т. 1. — с.249
- ↑ 2 Gollob MH, et al, 2001, N. Engl. J. Med. 344: 1823-1831.
- ↑ 1 2 3 Coban‐Akdemir Z. H. et al. Wolff–Parkinson–White syndrome: De novo variants and evidence for mutational burden in genes associated with atrial fibrillation //American Journal of Medical Genetics Part A. – 2020.
Литература
править- Вольфа-Паркинсона-Уайта синдром / Лирман А. В. // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский. — 3-е изд. — М. : Советская энциклопедия, 1977. — Т. 4 : Валин — Гамбия. — 576 с. : ил.