Активные формы кислорода (АФК, реактивные формы кислорода, РФК, англ. Reactive oxygen species, ROS) — включают ионы кислорода, свободные радикалы и перекиси как неорганического, так и органического происхождения. Это, как правило, небольшие молекулы с исключительной реактивностью благодаря наличию неспаренного электрона на внешнем электронном уровне.
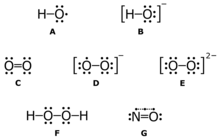
В живой клетке
правитьАФК постоянно образуются в живой клетке как продукты нормального метаболизма кислорода. Активные формы кислорода образуются также под действием ионизирующего излучения. Некоторые АФК могут играть роль медиаторов важных внутриклеточных сигнальных путей. Однако повышенная продукция АФК приводит к оксидативному стрессу. Нормальные функции АФК включают индукцию иммунной системы и мобилизацию систем ионного транспорта. Например, клетки крови на месте повреждения начинают продуцировать АФК, что рекрутирует тромбоциты, необходимые для начала процесса заживления раны. АФК также запускают программируемую клеточную смерть (апоптоз).
Антиоксидантная защита
правитьОколо 98 % от всего потребляемого клеткой кислорода восстанавливается в митохондриях до воды в процессе окислительного фосфорилирования, но 2 % за счёт побочных реакций, в основном в начале или в середине дыхательной цепи митохондрий, в том числе реакций, катализируемых цитохром с-оксидазой, превращаются сначала в частично восстановленный супероксид кислорода, а затем в гидроксильный радикал OH•, также относящийся к АФК[1]. Помимо митохондрий к образованию АФК в результате реакции Фентона может приводить накапливающийся в клетках липофусцин из-за своей способности соединяться с некоторыми переходными металлами[2][3]. Защита клетки от АФК осуществляется несколькими антиоксидантными ферментами (супероксиддисмутаза, каталаза и пероксиредоксины) и низкомолекулярными антиоксидантами (витамин С, глутатион, мочевая кислота). Кроме этого, антиоксидантными свойствами обладают полифенолы (например, ресвиратрол и другие компоненты красного вина).
См. также
правитьЛитература
править- Free Radicals in Biology and Medicine by B.Halliwell and M.C.Gutteridge. Oxford University Press, 2000
- Sen, C.K. (2003) The general case for redox control of wound repair, Wound Repair and Regeneration, 11, 431—438
- Krötz, F., Sohn, HY., Gloe, T., Zahler, S., Riexinger, T., Schiele, T.M., Becker, B.F., Theisen, K., Klauss, V., Pohl, U. (2002) NAD(P)H oxidase-dependent platelet superoxide anion release increases platelet recruitment, Blood, 100, 917—924
- Pignatelli, P. Pulcinelli, F.M., Lenti, L., Gazzaniga, P.P., Violi, F. (1998) Hydrogen Peroxide Is Involved in Collagen-Induced Platelet Activation, Blood, 91 (2), 484—490
- Guzik, T.J., Korbut, R., Adamek-Guzik, T. (2003) Nitric oxide and superoxide in inflammation and immune regulation, Journal of Physiology and Pharmacology, 54 (4), 469—487
Примечания
править- ↑ Скулачёв В. П. Эволюция, митохондрии кислород // Соросовский образовательный журнал : журнал. — 1999. — № 9. Архивировано 30 августа 2018 года.
- ↑ Annika Höhn, Tobias Jung, Stefanie Grimm, Tilman Grune. Lipofuscin-bound iron is a major intracellular source of oxidants: role in senescent cells // Free Radical Biology & Medicine. — 2010-04-15. — Т. 48, вып. 8. — С. 1100–1108. — ISSN 1873-4596. — doi:10.1016/j.freeradbiomed.2010.01.030. Архивировано 1 сентября 2018 года.
- ↑ Jeannette König, Christiane Ott, Martín Hugo, Tobias Jung, Anne-Laure Bulteau. Mitochondrial contribution to lipofuscin formation // Redox Biology. — 2017-01-25. — Т. 11. — С. 673–681. — ISSN 2213-2317. — doi:10.1016/j.redox.2017.01.017.