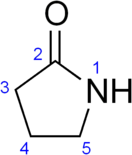
2-Пирролидон (γ-бутиролактам, пирролидин-2-он) — органическое соединение класса лактамов[2].
| Пирролидон | |||
|---|---|---|---|
| |||
| Общие | |||
| Хим. формула | C4H7NO | ||
| Физические свойства | |||
| Молярная масса | 85,11 г/моль | ||
| Плотность | 1,116 г/см³ | ||
| Энергия ионизации | 9,2 эВ[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 23—25 °C | ||
| • кипения | 245 °C | ||
| Давление пара | 12 (133°C)мм.рт.ст. | ||
| Классификация | |||
| Рег. номер CAS | 616-45-5 | ||
| PubChem | 12025 | ||
| Рег. номер EINECS | 210-483-1 | ||
| SMILES | |||
| InChI | |||
| RTECS | UY5715000 | ||
| ChEBI | 36592 | ||
| ChemSpider | 11530 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Физические свойства
правитьБесцветная жидкость с характерным запахом. Легко растворим в воде, спирте, бензоле, диэтиловом эфире, хлороформе, сероуглероде. Плохо растворим в петролейном эфире. Для очистки в лаборатории используют перекристаллизацию из петролейного эфира.[3]
Методы синтеза
править- Из гамма-бутиролактона реакцией с аммиаком под давлением[4].
- Гидрированием сукциннитрила в пиридине с последующей обработкой образовавшегося аминонитрила.
- Альтернативный метод — частичное гидрирование сукцинимида.
Применение
правитьИспользуется как полупродукт в синтезе:
- поливинилпирролидона (получаемый реакций с ацетиленом при катализе калием и нагреванием до 100 °C)[5],
- пирацетама.
Как полярный высококипящий растворитель в промышленности. В картриджах для струйной печати[6].
Биологическая роль
правитьПирролидоновый цикл входит в структуру ноотропных препаратов рацетамовой группы:
- Котинин,
- Пирацетам,
- Этосуксимид,
- Прамирацетам и др.
Безопасность
правитьМалоопасное вещество при внутрижелудочном поступлении в организм, 4 класс опасности. Обладает умеренной способностью к кумуляции. Раздражает кожу и слизистые оболочки глаз. Проникает через неповрежденные кожные покровы. Пирролидон обладает эмбриотоксическим, тератогенным и мутагенным действием (при сверхвысоких концентрациях).
Примечания
править- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ Берестовицкая В.М., Васильева О.С., Остроглядов Е.С. 2-Пирролидон и его производные. Монография. СПб.: Астерион. 2013. elibrary.ru. Дата обращения: 17 февраля 2017.
- ↑ Справочник химика. - Т.2. - Л.-М.: Химия, 1964. - С. 896-897
- ↑ Вацулик П. Химия мономеров. Том I. М., ИЛ, 1960.
- ↑ W. Reppe: Vinylierung, in: Justus Liebigs Ann. Chem., 1956, 601, S. 81–138.
- ↑ Safety Data Sheet (PDF). HP website. HP (7 октября 2014). Дата обращения: 11 октября 2014. Архивировано из оригинала 16 октября 2014 года.
Это заготовка статьи об органическом веществе. Помогите Википедии, дополнив её. |