Оксиметилфурфурол (ОМФ) — промежуточный продукт химического разложения сахаров.[1] Легко образуется из моносахаридов в кислой среде.[2] Химическая формула C6H6O3. Присутствует во всей выпечке, где образуется из гексоз, также образуется при разложении мёда при его разбавлении горячей водой[3].
| Оксиметилфурфурол | |
|---|---|
 | |
| Общие | |
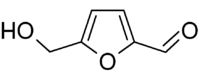
| Систематическое наименование |
5-гидроксиметилфурфурол |
| Хим. формула | C6H6O3 |
| Физические свойства | |
| Молярная масса | 126,11 г/моль |
| Плотность | 1,29 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 30–34 °C |
| • кипения | 114–116 (1 мбар) °C |
| Классификация | |
| Рег. номер CAS | 67-47-0 |
| PubChem | 237332 |
| Рег. номер EINECS | 200-654-9 |
| SMILES | |
| InChI | |
| RTECS | LT7031100 |
| ChEBI | 412516 |
| ChemSpider | 207215 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Физические свойства
правитьЛегкоплавкие бесцветные или желтоватые кристаллы. Продажный продукт — бесцветная жидкость, буреющая при хранении.[4] Смешивается с водой во всех соотношениях.
Получение
правитьОксиметилфурфурол получают из сахаров. Конкретнее получение проходит через стадию дегидратации фруктозы.[5] Обрабатывают кислотой водный раствор фруктозы, затем извлекают продукт экстракцией в системе жидкость-жидкость растворителем, например, метилизобутилкетоном. Добавки такие как ДМСО, 2-бутанол, поливинил пирролидон минимизируют образование побочных продуктов. Ионные жидкости облегчают получение окиметилфурфурола.[6]. Если для гидролиза используется соляная кислота, то образуется 5-хлорметилфурфурол вместо оксиметилфурфурола. Методика получения оксиметилфурфурола из сахарозы.[7] Хлорид хрома (II) катализирует прямую конверсию фруктозы (выход >90 %) и глюкозы (выход >70 %) в ОМФ.[8]
Химические свойства
правитьОкисление ОМФ даёт 2,5-фурандикарбоновую кислоту, которую можно использовать вместо терефталевой кислоты в производстве полиэфиров.
Применение
правитьОксиметилфурфурол образуется при разложении сахаров. Поэтому по его концентрации судят о качестве сахаросодержащих продуктов, например, определяют качество мёда. Содержание оксиметилфурфурола является одним из критериев для установления сроков хранения пчелиного мёда и для выявления его фальсификатов. В соответствии с ГОСТ 19792-2001 содержание ОМФ в 1 кг мёда не должно превышать 25 мг.[2]
Биохимия
правитьГлавный метаболит ОМФ в человеке - 5-гидроксиметил-2-карбоксифурановая кислота, которая выводится с мочой. ОМФ может также метаболизироваться в 5-сулфоксиметилфурфурол, который очень активен и может образовывать аддукты с ДНК или белками. In vitro тесты и изучение на крысах предполагает потенциальную токсичность и канцерогенность ОМФ.[9] На человеке корреляция между приёмом ОМФ и заболеваниями не обнаружена.[источник не указан 731 день]
Количественное определение
правитьЭталонным методом для количественного определения ОМФ является ВЭЖХ с УФ-детекцией. Классическим методом определения ОМФ является колориметрия с использованием бисульфитного восстановления либо с использованием p-толуидина и барбитуровой кислоты. Колориметрия является неспецифическим методом, так как затрагивает также родственные вещества. Поэтому результаты колориметрии несколько завышены по отношению к результатам ВЭЖХ. Существуют также тестовые наборы для определения наличия ОМФ.[10][11]
Безопасность
правитьЕсть данные о токсичности и мутагенности для крыс. Для человека не доказано[12].
Примечания
править- ↑ Что такое гидроксиметилфурфурол и чем он опасен? | Журнал без рекламы «Справочник потребителя». Дата обращения: 5 апреля 2011. Архивировано 3 марта 2011 года.
- ↑ 1 2 Архивированная копия. Дата обращения: 5 апреля 2011. Архивировано из оригинала 2 апреля 2015 года.
- ↑ Альбина Комиссарова. Меняем пищевое поведение! Худеем вместе. — Litres, 2020-03-11. — 247 с. — ISBN 978-5-04-174854-8. Архивировано 22 января 2021 года.
- ↑ ОКСИМЕТИЛФУРФУРОЛ. Дата обращения: 5 апреля 2011. Архивировано из оригинала 8 июля 2014 года.
- ↑ Yuriy Román-Leshkov, Juben N. Chheda, James A. Dumesic (2006). «Phase Modifiers Promote Efficient Production of Hydroxymethylfurfural from Fructose». Science 312 (5782): 1933—1937.
- ↑ Ståhlberg, T.; Fu, W.; Woodley, J. M.; Riisager, A. «Synthesis of 5-(Hydroxymethyl)furfural in Ionic Liquids: Paving the Way to Renewable Chemicals» ChemSusChem. 2011, Volume 4, pages 451—458.
- ↑ Методы получения химических реактивов и препаратов. Москва, ИРЕА, Выпуск 20, 1969, стр. 159
- ↑ Haibo Zhao, Johnathan E. Holladay, Heather Brown, Z. Conrad Zhang (2007). «Metal Chlorides in Ionic Liquid Solvents Convert Sugars to 5-Hydroxymethylfurfural». Science 316 (5782): 1597—1600.
- ↑ Husøy, T.; Haugen, M.; Murkovic, M.; Jöbstl, D.; Stølen, L.H.; Bjellaas, T.; Rønningborg, C.; Glatt, H.; Alexander, J. (2008). "Dietary exposure to 5-hydroxymethylfurfural from Norwegian food and correlations with urine metabolites of short-term exposure". Food and Chemical Toxicology 46 (12): 3697–702.
- ↑ Schultheiss, J.; Jensen, D.; Galensa, R. (2000). "Determination of aldehydes in food by high-performance liquid chromatography with biosensor coupling and micromembrane suppressors". Journal of Chromatography A 880: 233.
- ↑ Gaspar, Elvira M.S.M.; Lucena, Ana F.F. (2009). "Improved HPLC methodology for food control – furfurals and patulin as markers of quality". Food Chemistry 114 (4): 1576.
- ↑ Heat Forms Potentially Harmful Substance In High-fructose Corn Syrup, Bee Study Finds. Дата обращения: 4 февраля 2012. Архивировано 3 февраля 2012 года.
Это заготовка статьи об органическом веществе. Помогите Википедии, дополнив её. |
В другом языковом разделе есть более полная статья Hydroxymethylfurfural (англ.). |