Нитрит кальция — неорганическое соединение, соль кальция и азотистой кислоты с формулой Ca(NO2)2, бесцветные кристаллы, растворяется в воде, образует кристаллогидраты. Умеренно-токсичен. Относится к III классу опасности.
| Нитрит кальция | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Нитрит кальция |
| Традиционные названия | Нитрит кальция; азотистокислый кальций |
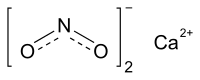
| Хим. формула | Ca(NO2)2 |
| Рац. формула | Ca(NO2)2 |
| Физические свойства | |
| Состояние | бесцветные кристаллы |
| Молярная масса | 132,09 г/моль |
| Плотность | 2,23 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 392 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | 82,613; 94,625; 180100 г/100 мл |
| Классификация | |
| Рег. номер CAS | 13780-06-8, 182893-14-7 |
| PubChem | 159695 и 11829479 |
| Рег. номер EINECS | 237-424-2 |
| SMILES | |
| InChI | |
| ChemSpider | 140414 |
| Безопасность | |
| Предельная концентрация | 5 мг/м³ |
| ЛД50 | 200-623 мг/кг |
| Токсичность | ирритант, среднетоксичен |
| Фразы безопасности (S) | S23, S24/25, |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Получение
править- Разложение нитрата кальция:
- Пропускание диоксида азота через суспензию гидроксида кальция:
Физические свойства
правитьНитрит кальция образует бесцветные (или слегка желтоватые) кристаллы.
Хорошо растворяется в воде, слабо растворяется в этаноле
.
Образует кристаллогидраты состава Ca(NO2)2•n H2O, где n = 1 и 4.
Литература
править- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- CRC Handbook of Chemistry and Physics[англ.]. — 89th Edition. — Taylor and Francis Group, LLC, 2008-2009.
Это заготовка статьи о неорганическом веществе. Помогите Википедии, дополнив её. |
