Ку-лихорадка (коксиеллёз, австралийский риккетсиоз, Ку-риккетсиоз, болезнь Дерика-Бернета, квинслендская лихорадка, среднеазиатская лихорадка, термезская лихорадка, пневмориккетсиоз) — острый природно-очаговый риккетсиоз[2], характеризующийся общетоксическими явлениями, лихорадкой и, нередко, атипичной пневмонией[3]. Наибольшему риску заражения подвергаются лица, ухаживающие за животными. Возбудитель — Coxiella burnetii[4]. Это кокковидные или коккобактериальные, полиморфные, неподвижные, аэробные микроорганизмы. Окрашиваются по способу Романовского-Гимзы. Культивируются при температуре 37 °C в желточных мешках развивающихся куриных эмбрионов, в асцитической жидкости или на сывороточном агаре[5].
| Ку-лихорадка | |
|---|---|
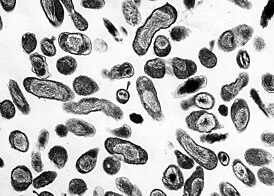 Coxiella burnetii | |
| МКБ-11 | 1C33 |
| МКБ-10 | A78 |
| МКБ-10-КМ | A78 |
| МКБ-9 | 083.0 |
| МКБ-9-КМ | 083.0[1] |
| DiseasesDB | 11093 |
| MedlinePlus | 001337 и 000611 |
| eMedicine | med/1982 |
| MeSH | D011778 |
Исторические сведения
правитьБолезнь впервые описал Е. Деррик в 1937 году. Он назвал её «Q-fever» (англ. query — сомнение). В том же году он выделил возбудителя, риккетсиозную природу которого через два года установил Ф. Бернет. В СССР эта болезнь была обнаружена в 1960-х годах.
Во время вспышки в декабре 2009 в Нидерландах ошибочно названа «козьим гриппом» из-за сходных симптомов[6]. В мае 2020 года вспышка Ку-лихорадки произошла в Болгарии, заболели 14 человек[7][8].
Этиология
правитьВозбудитель Coxiella burnetii относится к микроорганизмам, необычно устойчивым к окружающей среде, а также к различным физическим и химическим воздействиям, в том числе к дезинфицирующим средствам. При хлорировании воды и кипячении в течение 10 мин возбудитель гибнет.
Эпидемиология
правитьПредположительно, эта страница или раздел нарушает авторские права. |
Различают сельскохозяйственные и природные очаги болезни. В с.-х. очагах источниками возбудителя инфекции являются крупный и мелкий рогатый скот, лошади, свиньи, собаки, домашние птицы, грызуны; в природных очагах — дикие копытные и мелкие млекопитающие животные, в основном грызуны, птицы. Основное эпидемиологическое значение имеют млекопитающие — крупный и мелкий рогатый скот, свиньи и др., выделяющие риккетсии с испражнениями, мочой, молоком, околоплодными водами. Заражение людей: в с.-х. очагах происходит воздушно-пылевым путём при обработке загрязнённых животными шерсти, пуха, меха, щетины, кожи; пищевым путём при употреблении в пищу загрязнённого молока и молочных продуктов, через загрязнённые руки; при контакте с инфицированными животными во время ухода за ними, их убое и разделке туш.
В природных очагах возбудители передаются трансмиссивным путём — клещами, в основном иксодовыми, в меньшей мере аргасовыми, гамазовыми, краснотелковыми (см. Клещи). Риккетсии способны длительно сохраняться в организме иксодовых и аргасовых клещей и передаются трансовариально и трансфазово (яйцо, личинка, нимфа, взрослый клещ), что позволяет считать этих клещей не только переносчиками, но и резервуаром возбудителя лихорадки. Заболеваемость: преимущественно спорадическая, регистрируется среди групп профессионального риска (животноводы), среди сельских жителей, в основном в весенне-летне-осеннее время года. Возможны и эпидемические вспышки. Заражение от больного человека происходит редко — через инфицированную мокроту и молоко кормящих женщин.
Патогенез
правитьНизкая доза (от 1 до 10 бактерий) может вызвать инфекцию. Инкубационный период составляет приблизительно две-три недели (диапазон: от одной до шести недель). После попадания заражённых частиц в организм хозяина микроорганизм размножается в фаголизосомах макрофагов и моноцитов, что позволяет им избежать фагоцитоза. Если бактерия попала путём ингаляции, то её в организме переносят преимущественно легочные макрофаги в печень, селезёнку и костный мозг. Системная инвазия бактерий в организм хозяина приводит к появлению симптомов и различных клинических проявлений, которые зависят от инфицирующей дозы и реакции организма хозяина. У иммунокомпетентных пациентов воспалительный ответ может быть вызван иммунными механизмами, которые проявляются в виде образования без некротических гранулем в печени или костном мозге, известных как пончико-подобные гранулемы.
У небольшой части пациентов первичное инфицирование приводит к персистирующей очаговой инфекции. Такие изменения зависят как от факторов, связанных с организмом хозяина, так и бактерий. Например, у небольшого числа пациентов макрофаги не способны убить микроорганизм из-за повышенной секреции интерлейкина (IL) -10, который продуцируется инфицированными моноцитами. У пациентов с персистирующей очаговой инфекцией наблюдаются высокие уровни интерлейкина-10. К пациентам с риском развития персистирующей очаговой инфекции относят беременных и пациентов с ранее существовавшей вальвулопатией или васкулопатией, а также иммунокомпрометированных больных вследствие ВИЧ-инфекции или проведения химиотерапии при онкологических заболеваниях.
Хотя жизненный цикл возбудителя остается неясным, существует две формы микроорганизма (малая и большая), которые легко различить с помощью электронной микроскопии. Малая форма микроорганизма («псевдоспора») устойчива к нагреванию, высыханию и множественным дезинфицирующим средствам, что позволяет возбудителю оставаться жизнеспособным в течение длительного периода времени. Например, бактерии могут выживать при низких температурах в хранящемся мясе в течение одного месяца и в обезжиренном молоке при комнатной температуре в течение 40 месяцев.
C. burnetii имеет два антигенных состояния. Бактерии, выделенные от пациентов или лабораторных животных, находятся в фазе I антигена, и такой микроорганизм считается вирулентным. Бактерия, выделенная из субкультур клеток или яиц с эмбрионами, имеет антигенный сдвиг и находится в фазе II антигена, и является авирулентной формой. Бактерии, которые находятся в фазе I и II антигена содержат плазмиды, но их роль в патогенезе болезни недостаточно изучена. Для подтверждения диагноза болезни определяют антитела к антигенам фазы I и II микроорганизма. Только 1-2% пациентов умирают от острой формы инфекции. Те, кто полностью выздоравливает, могут обладать пожизненным иммунитетом против реинфекции (иммунитет является нестерильным, случаи реинфекции не были зарегистрированы). Тем не менее, до 65% людей с нелеченным эндокардитом могут умереть от этой болезни[9].
Клиническая картина
правитьИнкубационный период: от 3 до 32 дней, чаще 12—19 дней. В большинстве случаев болезнь начинается остро. Жалобы разнообразны: головная боль, боли в пояснице, мышцах, суставах, чувство разбитости, сухой кашель, потливость, потеря аппетита, нарушение сна. При осмотре выявляются гиперемия лица, инъекция сосудов склер, гиперемия зева. У большинства больных рано появляется гепатолиенальный синдром. Температура — 39—40°, температурная кривая разнообразная — постоянная, ремиттирующая, волнообразная, неправильная. Продолжительность лихорадки: чаще в пределах 2 недель, однако возможны рецидивы, затяжная субфебрильная лихорадка. У части больных выявляются пневмония, трахеобронхит (при воздушно-пылевом пути заражения). Картина крови мало характерна; чаще отмечаются лейко- и нейтропения, относительный лимфоцитоз, умеренное увеличение СОЭ. Выделяют острую (до 2—3 нед.), подострую (до 1 мес.) и хроническую (до 1 года) формы, а также стертую форму, которая диагностируется лишь в очагах при лабораторном обследовании. Осложнения редки.
Диагностика
правитьДиагноз Ку-лихорадки основывается на клинической картине, данных эпидемиологического анамнеза (учёт профессии и эндемичности болезни) и результатах лабораторных исследований (используются реакции связывания комплемента, агглютинации, непрямой иммунофлюоресценции, кожная аллергическая проба).
Лечение
править21-дневный курс пероральной антибиотикотерапии
править- Острая инфекция обычно протекает мягко, имеет тенденцию к самоограничению и обычно спонтанно разрешается в течение двух недель.
- Лечение не рекомендовано пациентам с острой инфекцией без вальвулопатии, у которых нет симптомов. Однако при наличии симптомов, следует проводить пероральную антибиотикотерапию, поскольку она может сократить продолжительность заболевания и снизить риск госпитализации.
- Рекомендуемая терапия первой линии — доксициклин (см. Тетрациклины). Если пациент не переносит доксициклин, можно использовать другие антибиотики (например, фторхинолоны или триметоприм / сульфаметоксазол).
- Курс лечения составляет от 14 до 21 дня.
Плюс — Поддерживающая терапия
править- Пациентам с острой инфекцией следует соблюдать постельный режим и пить много жидкости.
- При кашле можно использовать противокашлевые средства
- Парацетамол или нестероидные противовоспалительные препараты (НПВП) не рекомендуются для лечения лихорадки и дискомфорта, поскольку они могут ухудшить функцию печени, и, соответственно, усугубить болезнь[9].
Прогноз
правитьЭтот раздел не завершён. |
Прогноз заболевания благоприятный, летальные исходы редки.
Профилактика
правитьПрофилактика Ку-лихорадки: заключается в проведении комплекса санитарно-ветеринарных и санитарно-профилактических мероприятий. Они направлены на предотвращение заноса инфекции в животноводческие хозяйства и включают осмотр и обследование вновь поступающих в хозяйство животных, изоляцию и лечение больных животных, обеззараживание их испражнений и околоплодных вод, а также помещений (стойла, кормушки и т. п.) 3—5 % раствором креолина или 10—20 % раствором хлорной извести. При работе с больными животными (уход, лечение) следует соблюдать меры личной профилактики — пользоваться специальной одеждой (резиновыми сапогами, перчатками, фартуками, марлевыми респираторами с дезинфекцией их после работы). Молоко из неблагополучных хозяйств обязательно стерилизуют, приготовление кефира, творога, масла и др. из некипяченого молока недопустимо. В эпидемиологическом очаге Ку-лихорадки проводят текущую и заключительную дезинфекцию, по эпидемическим показаниям — вакцинацию людей. Важное значение имеет гигиеническое воспитание населения в отношении профилактики Ку-лихорадки.
Применение в качестве бактериологического оружия
правитьВозбудитель Ку-лихорадки использовался в СССР во Второй мировой войне в качестве бактериологического оружия. Разработка велась в Научно-исследовательском институте эпидемиологии и гигиены (в настоящий момент — НИИ микробиологии МО РФ) в г. Кирове[10]. По предположению некоего подполковника, упоминающегося в книге Канатжана Алибекова, вспышка Ку-лихорадки в рядах немецких войск в Крыму была вызвана применением соответствующей риккетсии[11]. До этого случая на территории Советского Союза заболевания Ку-лихорадкой известны не были[10].
Примечания
править- ↑ Disease Ontology (англ.) — 2016.
- ↑ Coxiella burnetii не относятся к бактериям семейства Rickettsiales
- ↑ Е.П.Шувалов, Е.С. Белозеров. Инфекционные болезни. — 2016.
- ↑ Е. П. Шувалова. Инфекционные болезни. — Медицина, 2005. — ISBN 522-504-00-63.
- ↑ Р.Ф.Сосов и др. Эпизоотология. — М.: Колос, 1969. — 400 с.
- ↑ Грипп, который не грипп. Дата обращения: 15 декабря 2009.
- ↑ Черен Пипер. В Болгарию пришла ку-лихорадка. bourgas.ru. Дата обращения: 25 сентября 2020.
- ↑ BgNews-Новости Болгарии. В Болгарии выявлены два очага ку-лихорадки. Новости Болгарии (11 июня 2020). Дата обращения: 25 сентября 2020. Архивировано 17 июня 2020 года.
- ↑ 1 2 Инфекции Coxiella burnetii: симптомы, диагностика, профилактика и лечение. Дата обращения: 9 мая 2019. Архивировано 9 мая 2019 года.
- ↑ 1 2 Советское биологическое оружие: история, экология, политика Архивная копия от 13 ноября 2013 на Wayback Machine, Л. А. Фёдоров, Москва 2005
- ↑ Alibek, Ken. Biohazard : the chilling true story of the largest covert biological weapons program in the world, told from the inside by the man who ran it. — 1st ed. — New York: Random House, 1999. — С. 36. — xi, 319 pages, 8 unnumbered pages of plates с. — ISBN 9780375502316. Архивировано 17 апреля 2020 года.
Литература
править- Лобан К. М. Лихорадка Ку (коксиеллез). — М.: Медицина, 1987. — 128 с. — 13 000 экз.
- Руководство по инфекционным болезням / Под ред. В. И. Покровского и К. М. Лобана. — М., 1986. — С. 204.