Тиосульфа́ты — соли и сложные эфиры тиосерной кислоты, H2S2O3. Тиосульфаты неустойчивы, поэтому в природе не встречаются. Наиболее широкое применение имеют тиосульфат натрия и тиосульфат аммония.
История открытия и исследования
правитьОрганические тиосульфаты были исследованы немецким химиком Гансом Бунте в 1872 году[1] в его докторской диссертации.
Строение
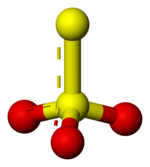
правитьТиосульфат-ион по строению близок к сульфат-иону. В тетраэдре [SO3S]2− связь S−S (1,97 Å) длиннее, чем связи S−O (1,48 Å).
Физические свойства
правитьРастворимость в воде (г/100 г):
- K2S2O3 200,1 (35 °C), 233,4 (56 °C)
- (NH4)2S2O3 173 (20 °C)
- MgS2O3 49,8 (20 °C)
- CaS2O3 42,9 (10 °C)
- SrS2O3 15,3 (10 °C)
- BaS2O3 0,2 (0 °C)
- Tl2S2O3 0,18 (25 °C)
- PbS2O3 0,02 (18 °C)
Образуют кристаллогидраты, при нагревании которых происходит плавление, представляющее собой растворение тиосульфатов в кристаллизационной воде.
- К2S2O3·5Н2О — температура плавления 35,0 °C
- К2S2O3·3Н2О — температура плавления 56,1 °C
- K2S2O3·H2О — температура плавления 78,3 °C, плотность 2,590 г/см³
- MgS2O3·6H2O — температура плавления выше 82 °C, плотность 1,818 г/см³
- CaS2O3·6H2O — температура плавления выше 40 °C, плотность 1,872 г/см³
Получение
правитьТиосульфаты получаются при взаимодействии растворов сульфитов с сероводородом:
При кипячении растворов сульфитов с серой:
При окислении полисульфидов кислородом воздуха:
Химические свойства
правитьТиосерная кислота H2S2O3 в присутствии воды разлагается:
поэтому её выделение из водного раствора невозможно. Свободная тиосерная кислота может быть получена при взаимодействии хлорсульфоновой кислоты с сероводородом при низкой температуре:
Выше 0 °C свободная тиосерная кислота необратимо разлагается по вышеприведённой реакции.
Благодаря наличию серы в степени окисления −2 тиосульфат-ион обладает восстановительными свойствами. Слабыми окислителями (I2, Fe3+) тиосульфаты окисляются до тетратионатов:
Более сильные окислители окисляют тиосульфаты до сульфатов:
Сильные восстановители восстанавливают тиосульфат-ион до сульфида, например:
Тиосульфат-ион также является сильным комплексообразователем:
Так как тиосульфат-ион координируется с металлами через атом серы в степени окисления −2, в кислой среде тиосульфатные комплексы легко переходят в сульфиды:
Из-за наличия атомов серы в разных степенях окисления в кислой среде тиосульфаты склонны к реакциям диспропорционирования:
Применение
правитьТиосульфаты используются в:
- фотографии в качестве компонента фиксажа
- аналитической и органической химии
- горнорудной промышленности
- текстильной и целлюлозно-бумажной промышленности
- пищевой промышленности
- Химчистке
- медицине
Фотография
правитьИспользование тиосульфата натрия в фотографии в качестве фиксажа основано на способности тиосульфат-иона переводить нерастворимые в воде светочувствительные галогениды серебра в растворимые несветочувствительные комплексы:
Фиксажи условно делятся на нейтральные, кислые, дубящие и быстрые.
Нейтральный фиксаж представляет собой раствор тиосульфата натрия в воде (250 г/л). Для более быстрого прекращения действия проявляющих веществ, занесённых из проявителя в эмульсионном слое во избежание появления вуали на изображении фиксирование обычно проводят в слабокислой среде. В качестве подкислителей используют серную и уксусную кислоты, а также гидросульфит или метабисульфит (K2S2O5) калия.
Для упрочнения эмульсионного слоя используют дубящие фиксажи. В качестве дубящих веществ в разных рецептурах могут использоваться тетраборат натрия (бура), борная кислота (одновременно как подкислитель), хромокалиевые или алюмокалиевые квасцы и формалин.
Скорость реакции комплексообразования уменьшается от AgCl к AgI, поэтому при использовании бромсеребряных и иодсеребряных фотоматериалов используются быстрые фиксажи на основе тиосульфата аммония. Ускорение процесса фиксирования происходит за счёт промежуточной стадии — быстро протекающего образования аммиачного комплекса серебра:
Из-за гигроскопичности тиосульфата аммония обычно применяют смесь тиосульфата натрия и хлорида аммония.
Химия
правитьВ аналитической химии тиосульфат натрия используется в качестве реагента в иодометрии. Его использование основано на реакции окисления тиосульфат-иона иодом до тетратионата:
Растворы тиосульфата натрия нестабильны из-за взаимодействия с углекислым газом, содержащемся в воздухе и растворённом в воде:
и вследствие окисления кислородом воздуха:
и в результате контаминации растворов тионовыми бактериями, которые окисляют тиосульфаты до сульфатов, осуществляя хемосинтез. Поэтому приготовление раствора тиосульфата натрия из навески нецелесообразно. Обычно готовят раствор приблизительной концентрации и устанавливают точную концентрацию титрованием раствором бихромата калия или иода.
При иодометрическом титровании применяют метод обратного титрования, то есть прибавляют избыток раствора иодида калия точной концентрации, а затем титруют образовавшийся иод раствором тиосульфата натрия..
Горнорудная промышленность
правитьВ горнорудной промышленности тиосульфат натрия используется для извлечения серебра и золота из руд и минералов как альтернатива цианидному выщелачиванию
Процесс тиосульфатного выщелачивания основан на окислении золота и серебра кислородом воздуха в присутствии тиосульфата натрия (тиосульфатное выщелачивание):
в кислой среде или двухвалентной медью:
в щелочной среде (тиосульфатно-аммиачное выщелачивание).
Аналогичные процессы происходят и при выщелачивании серебра.
Преимуществами тиосульфатно-аммиачного выщелачивания перед цианидным является отсутствие необходимости в использовании высокотоксичных реагентов, а также более полное извлечение металлов из руд, содержащих большие количества меди и марганца. При тиосульфатно-аммиачном выщелачивании в рабочий раствор добавляют серу и сульфит аммония, что позволяет обеспечить извлечение золота до 50—95 %
Текстильная промышленность
правитьПосле отбеливания тканей хлором их обрабатывают тиосульфатом натрия для удаления следов хлора и придания прочности:
Пищевая промышленность
правитьВ пищевой промышленности тиосульфат натрия применяется как пищевая добавка Е539 (регулятор кислотности).
Химчистка
правитьПри химчистке текстильных и кожных изделий тиосульфат натрия используется для удаления пятен, вызванных галогенами и их соединениями: йод, соединения хлора, бром.
Медицина
правитьВ медицине тиосульфат натрия используется:
- как антидот при отравлениях тяжёлыми металлами (ртуть, свинец, мышьяк), цианидами, солями иода и брома, лекарственными средствами[2], а также при детоксикации больных с алкогольными психозами;
- при лечении аллергических заболеваний, артрита и невралгии;
- при лечении кожных заболеваний (чесотка, псориаз).
тиосульфат магния — лекарственное средство при некоторых сердечно-сосудистых заболеваниях, вегетативных расстройствах.
Примеры
править- Тиосульфат рубидия образует кристаллогидраты состава Rb2SO3S•H2O и Rb2SO3S•2H2O
- Тиосульфат свинца(II) не растворяется в воде
См. также
правитьПримечания
править- ↑ Stiftung Werner-von-Siemens-Ring||C. ENGLER / H. BUNTE Архивировано 18 февраля 2009 года.
- ↑ Яцинюк Б. Б., Сенцов В. Г., Долгих В. Т. Коррекция гемодинамических нарушений тиосульфатом натрия при острых отравлениях пропранололом // Вестник Уральской медицинской академической науки. — 2011. — № 1(33). — С. 112—114.
Литература
править- Спиридонов Ф. М., Зломанов В. П. 13.1 Тиосерная кислота и тиосульфаты // Химия халькогенов. Учебное пособие. — М.: МГУ, 2000.
- Пилипенко А. Т., Пятницкий И. В. Иодометрия // Аналитическая химия. — М.: Химия, 1990. — С. 417—421. — 848 с. — ISBN 5-7245-0507-X.
- Аренс В. Ж. Геотехнологические методы добычи полезных ископаемых. — М.: Недра, 1975. — Т. 3. — С. 245—254. — 480 с.
- Фиксирование проявленных изображений.
- Спиридонов Ф. М., Зломанов В. П. Химия халькогенов Архивная копия от 16 октября 2008 на Wayback Machine.
- Ю. Ю. Лурье. Справочник по аналитической химии. М.: Химия, 1979.
- Пилипенко А. Т., Пятницкий И. В. Аналитическая химия. М: Химия, 1990.
- Аренс В. Ж. Геотехнологические методы добычи полезных ископаемых. — М.: Недра, 1975.