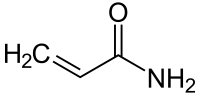
Акрилами́д (2-пропенамид) CH₂=CHC(O)NH₂ — амид акриловой кислоты, мономер, применяемый в основном в многотоннажном производстве важных полимеров, имеющих общее название полиакриламиды.
| Акриламид | |
|---|---|
 | |
| Общие | |
| Хим. формула | C3H5NO |
| Физические свойства | |
| Молярная масса | 71,08 г/моль |
| Плотность | 1,12 ± 0,01 г/см³[1] |
| Энергия ионизации | 9,5 ± 0,1 эВ[1] |
| Термические свойства | |
| Температура | |
| • плавления | 184 ± 1 ℉[1], 84 °C[2] и 84,5 °C[3] |
| • разложения | 572 ± 1 ℉[1] и 347 ± 1 ℉[1] |
| • вспышки | 280 ± 1 ℉[1] |
| • самовоспламенения | 424 ± 1 °C[4] |
| Давление пара | 0,007 ± 0,001 мм рт.ст.[1] |
| Классификация | |
| Рег. номер CAS | 79-06-1 |
| PubChem | 6579 |
| Рег. номер EINECS | 201-173-7 |
| SMILES | |
| InChI | |
| RTECS | AS3325000 |
| ChEBI | 28619 |
| Номер ООН | 2074 |
| ChemSpider | 6331 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Представляет собой бесцветные кристаллы с т. пл. 84,5°С, т. кип. 215°С, плотностью 1,122 г/см3. Растворяется в воде, этаноле, ацетоне. Мало растворим в бензоле. Слабо амфотерен. Пожароопасен и взрывоопасен. Токсичен — поражает нервную систему, печень и почки: ЛД50 составляет 149 мг/кг (крысы, перорально); ПДК 0,3 мг/м3. Раздражает слизистые оболочки.
В жареных или запечённых продуктах, а также выпечке акриламид может образовываться в реакции между аспарагином и сахарами (фруктоза, глюкоза, и т.д.) при температурах выше 180 °C[5]. Исследования обнаружили акриламид в черных оливках, сушеных сливах, арахисе, жареном картофеле, кофе.
Полимеризуется с образованием полиакриламида. Сополимеризуется с другими мономерами — стиролом, винилиденхлоридом и др. Вступает в реакции, характерные для алифатических амидов карбоновых кислот. Легко присоединяет по двойной связи амины, спирты, кетоны и др.
В промышленности получают гидролизом акрилонитрила, в лаборатории — из акрилоилхлорида или акрилового ангидрида и аммиака.
Примечания
править- ↑ 1 2 3 4 5 6 7 http://www.cdc.gov/niosh/npg/npgd0012.html
- ↑ Bradley J., Williams A., Andrew S.I.D. Lang Jean-Claude Bradley Open Melting Point Dataset // (unknown type) — 2014. — doi:10.6084/M9.FIGSHARE.1031637.V2
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ http://www.cdc.gov/niosh/ipcsneng/neng0091.html
- ↑ Вездесущая реакция Майара Архивная копия от 30 мая 2015 на Wayback Machine // Химия и жизнь №2, 2012.
Литература
править- Савицкая М. Н., Холодова Ю. Д., Полиакриламид, К., 1969.
- Энциклопедия полимеров, т. I, М., 1972, с. 29-32.
