1,2-Дифтортетрахлорэтан
1,2-Дифтортетрахлорэтан — низший хлорфторуглерод, бесцветная прозрачная жидкость со слабым запахом гексахлорэтана. Относится к хладонам, производство и применение которых регулируется Монреальским протоколом. Торговая марка (СССР, РФ) — хладон 112.
| 1,2-дифтортетрахлорэтан | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
1,2-Дифтортетрахлорэтан |
| Традиционные названия | Хладон-112, Фреон-112, R-112 |
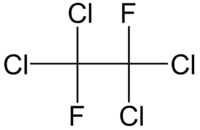
| Хим. формула | CFCl2CFCl2 |
| Рац. формула | C2Cl4F2 |
| Физические свойства | |
| Состояние | бесцветная жидкость |
| Молярная масса | 203,83 г/моль |
| Плотность | 1,65 ± 0,01 г/см³[1] |
| Энергия ионизации | 11,3 ± 0,1 эВ[1][2] |
| Термические свойства | |
| Температура | |
| • плавления | 26° |
| • кипения | 92,8° °C |
| Критическая точка |
285,5° давление: плотность: |
| Давление пара | 40 ± 1 мм рт.ст.[1] |
| Оптические свойства | |
| Показатель преломления | 1,413 ± 0,0001 |
| Классификация | |
| Рег. номер CAS | 76-12-0 |
| PubChem | 6427 |
| Рег. номер EINECS | 200-935-6 |
| SMILES | |
| InChI | |
| RTECS | KI1420000 |
| ChemSpider | 6187 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Свойства
правитьФизические свойства
правитьДостаточно инертная бесцветная жидкость. При ультрафиолетовом облучении в присутствии кислорода разрушается с образованием радикалов, которые дисмутируют до фторхлоруглеродов, хлоруглеродов и хлора (в том числе атомарного, взаимодействующего с озоном, что приводит к снижению концентрации озона в стратосфере).
Химические свойства
правитьОсновными химическими свойствами являются:
- 1,2-дифтортетрахлорэтан — нетоксичен, но вдыхание воздуха с его большими концентрациями может привести к отёку лёгких, вызывает наркотический эффект;
- взаимодействуя с водородом, образуют продукты замещения галогенов на водород;
- взаимодействуя с фтороводородом в присутствии катализаторов образуются продукты замещения хлора на фтор;
- плохо растворим в воде, не взаимодействует с ней;
- вещество растворяется в спирте, эфире и бензине;
- его химические превращения требуют высоких температур[3].
Получение
правитьОсновными промышленными методами производства 1,2-дифтортетрахлорэтана являются жидко- или газофазное фторирование 1,1,2,2-Тетрахлорэтана фтором, безводным фтороводородом в присутствии галогенидов сурьмы, гексахлорэтана фторидами металлов, а также дисмутация полифторхлоралкана при 150—250 °С в присутствии оксида или хлорида алюминия.
Применение
править1,2-Дифтортетрахлорэтан является инертным растворителем и реагентом для фторорганического синтеза. Применяется как чистящее средство.
Не токсичен для животных, не раздражает кожу и слизистые оболочки, поэтому в ветеринарии используется для достижения антигельминтного результата. Он эффективен в отношении гельминтов трематод (фасциолёза и парамфистоматоза), но действует исключительно на взрослые формы фасциолёз[4].
Примечания
править- ↑ 1 2 3 http://www.cdc.gov/niosh/npg/npgd0596.html
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 1,2-ДИФТОРТЕТРАХЛОРЭТАН. Информационный ресурс «Russian-chemistry.». Дата обращения: 11 июня 2019. Архивировано из оригинала 1 августа 2013 года.
- ↑ ДИФТОРТЕТРАХЛОРЭТАН DIFLUORTETRACHLORAETHANUM. Информационный ресурс «Животноводство». Дата обращения: 11 июня 2019. Архивировано 26 мая 2019 года.