Флуорен
Флуорен (о, о’-дифениленметан, трицикло-[7.4.0.02,7]-тридека-2,4,6,9,11,13-гексаен) — полициклический ароматический углеводород.
| Флуорен | |
|---|---|
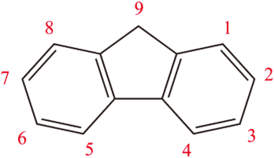 | |
| Общие | |
| Систематическое наименование |
Флуорен |
| Хим. формула | C13H10 |
| Физические свойства | |
| Молярная масса | 166,2 г/моль |
| Плотность | 1,181 г/см³ |
| Энергия ионизации | 7,89 эВ[1] |
| Термические свойства | |
| Температура | |
| • плавления | 116-117 °C |
| • кипения | 293-295 °C |
| Энтальпия | |
| • образования | 121 кДж/моль |
| Классификация | |
| Рег. номер CAS | 86-73-7 |
| PubChem | 6853 |
| Рег. номер EINECS | 201-695-5 |
| SMILES | |
| InChI | |
| RTECS | LL5670000 |
| ChEBI | 28266 |
| ChemSpider | 6592 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Свойства
правитьФлуорен представляет собой бесцветные кристаллы, способные к флуоресценции при действии ультрафиолетового облучения. В воде нерастворим, но хорошо растворяется в диэтиловом эфире, плохо растворим в этаноле.
Легко окисляется в положение 9: кислородом воздуха до 9-гидропероксифлуорена, при действии сильных окислителей — до флуоренона. При действии восстановителей (иодоводород, красный фосфор) образует пергидрофлуорен.
Флуорен образует карбанион в положении 9, в частности, конденсируется с ароматическими аминами с образованием 9-арилиденфлуоренов, при нагревании с металлическим натрием или амидом натрия образуется 9-натрийпроизводное флуорена.
Флуорен вступает также в реакции электрофильного замещения, при этом замещается атом водорода преимущественно в положения 2 и 7, затем в положение 4.
Нахождение в природе и получение
правитьФлуорен обнаруживается в каменноугольной смоле (1,3—2,0 %), из которой выделяется в составе антраценовой фракции кристаллизацией с последующей перекристаллизацией из бензина. Лабораторный синтез флуорена заключается в пиролизе ацетилена или дифенилметана.
Применение
правитьФлуорен служит исходным реагентом для целого ряда флуореновых красителей. Он также используется в качестве стабилизатора полимеров, а также как мономер. Монокристаллы флуорена используются в сцинтилляционных счётчиках.
Литература
править- Химическая энциклопедия / Редкол.: Зефиров Н.С. и др.. — М.: Большая Российская энциклопедия, 1998. — Т. 5 (Три-Ятр). — 783 с. — ISBN 5-85270-310-9.
Примечания
править- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
