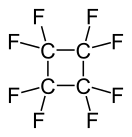
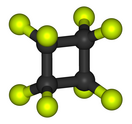
Октафторциклобутан
Октафторциклобута́н (перфторциклобутан, циклооктафторбутан, фреон C318, хладон C318) — фторорганическое соединение состава C4F8. Бесцветный, нетоксичный газ. Применяется как хладагент в холодильных системах или как рабочий газ при плазмохимическом травлении кварца[2].
| Октафторциклобутан | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
Октафторциклобутан | ||
| Традиционные названия | Перфторциклобутан, циклооктафторбутан | ||
| Хим. формула | C4F8 | ||
| Физические свойства | |||
| Состояние | газ | ||
| Молярная масса | 200,03 г/моль | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −41,4 °C | ||
| • кипения | −5,85 °C | ||
| • разложения | 550 °C | ||
| Критическая точка | 117 | ||
| Энтальпия | |||
| • образования | −1513 кДж/моль | ||
| Структура | |||
| Дипольный момент | 0 Кл·м[1] | ||
| Классификация | |||
| Рег. номер CAS | 115-25-3 | ||
| PubChem | 8263 | ||
| Рег. номер EINECS | 204-075-2 | ||
| SMILES | |||
| InChI | |||
| Кодекс Алиментариус | E946 | ||
| ChEBI | 31007 | ||
| ChemSpider | 13846040 | ||
| Безопасность | |||
| Предельная концентрация | 3000 мг/м³ | ||
| ЛД50 | 36 000 мг/кг (крысы, внутривенно) | ||
| Токсичность | не токсичен | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Получение
править- Электрохимическое фторирование тетрафторциклобутана.
- Циклодимеризация тетрафторэтилена.
- Пиролиз и разгонка полифторсодержащих органических веществ.
Химические свойства
правитьПри 700—725 °C в графитовой трубке пиролизуется до перфторизобутилена и гексафторпропена. При разбавлении аргоном и высокой температуре (830—990 °C) образуется в основном тетрафторэтилен.
При высокой температуре (340—360 °C) реагирует со фтором с образованием декафторбутана и продуктов расщепления углеродной цепи.
Примечания
править- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ https://docs.cntd.ru_Octafluorocyclobutanum
Литература
править- Вредные химические вещества: Углеводороды, галогенпроизводные углеводородов. Справочник. — Л.: Химия, 1990. — С. 299—300, 692—693.
- Новое в технологии соединений фтора. — М.: Мир, 1984. — С. 61, 63, 166—168.
- Промышленные фторорганические продукты: Справочник. — Л.: Химия, 1990. — С. 187—194.
- Химическая энциклопедия. — Т. 5. — М.: Советская энциклопедия, 1999. — С. 278—280.
- Mackay D., Shiu W. Y., Ma K.-C., Lee S. C. Handbook of Physical-Chemical Properties and Enviromental Fate for Organic Chemacals. — 2nd ed., Vol.2. — CRC Press, 2006. — С. 1211, 1214, 1219.
- Перри Дж. Справочник инженера-химика. В 2 т. — Т. 1. — Л.: Химия, 1969. — С. 69.