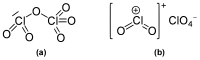
Дихлоргексаоксид (оксид хлора(V,VII), оксид хлора(VI), перхлорат хлорила) — бинарное неорганическое соединение хлора и кислорода с формулой Cl2O6. Представляет собой ярко-красную жидкость. В твёрдом состоянии является кристаллическим веществом оранжевого цвета. Жидкий дихлоргексаоксид имеет молекулярное строение: , кристаллический — ионное: .
| Дихлоргексаоксид | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Дихлоргексаоксид |
| Хим. формула | Cl2O6 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 166,901 г/моль |
| Плотность | 1,65 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 3 °C |
| • кипения | 203 °C |
| • разложения | 200 °C |
| Энтальпия | |
| • образования | +310 кДж/моль |
| Классификация | |
| Рег. номер CAS | 12442-63-6 |
| SMILES | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Получение
правитьДихлоргексаоксид получают окислением диоксида хлора озоном:
Свойства
правитьДихлоргексаоксид является нестойким веществом и начинает разлагаться уже при температурах 0—10 °C
При температурах выше 20 °C в продуктах распада появляется хлор.
С водой реагирует бурно — со вспышкой, при этом продуктами реакции являются хлорноватая и хлорная кислоты:
Взаимодействует с водой и щелочами в растворе, при этом проходит реакция диспропорционирования:
Проявляет сильные окислительные свойства:
Применяется в неорганическом синтезе для получения безводных перхлоратов металлов обменными реакциями. С AlCl3 образует ClO2[Al(ClO4)4], с FeCl3 — ClO2[Fe2(ClO4)7].
Литература
править- Зефиров Н.С. и др. т.5 Три-Ятр // Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1998. — 783 с. — ISBN 5-85270-310-9.

![{\displaystyle {\mathsf {[ClO_{2}]^{+}[ClO_{4}]^{-}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0201b414b4516573cdfb772bc5583f00e770e8c8)