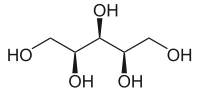
Ксилит или Ксилитол, CH2OH(CHOH)3CH2OH — многоатомный спирт (пентанпентаол). Натуральный сахарозаменитель.[1]
| Ксилит | |
|---|---|
 | |
| Общие | |
| Хим. формула | C5H12O5 |
| Физические свойства | |
| Молярная масса | 152,15 г/моль |
| Плотность | 1,52 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 94 °C[1] |
| • кипения | 216 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | 63 г/100 г (при 20 °C) |
| Классификация | |
| Рег. номер CAS | 87-99-0 |
| Рег. номер EINECS | 201-788-0 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E967 |
| ChEBI | 17151 |
| ChemSpider | 6646 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |

Свойства
правитьБесцветные гигроскопические кристаллы сладкого вкуса, растворимые в воде, спирте, гликолях, уксусной кислоте и пиридине. Вследствие сильной гигроскопичности ксилита, при его растворении в воде происходит охлаждение раствора. Энтальпия растворения составляет примерно −146,4 Дж/г. Показатель преломления 10%-ного водного раствора ксилита при 25 °C составляет 1,3471, а показатель преломления 50%-ного раствора — 1,4132[источник не указан 1489 дней]. Ксилит не имеет реакционноспособной карбонильной группы, поэтому не карамелизируется.
Получение
правитьКсилит может быть получен из растительного сырья, богатого полисахаридом ксиланом, например, из берёзовой древесины, миндальной шелухи, соломы, кукурузного початка, шелухи овса[2], либо из побочных продуктов производства целлюлозы. Сырьё, содержащее ксилан, гидролизуют до ксилозы методом кислотного гидролиза. Ксилозу далее разделяют хроматографическими методами и гидрируют с катализатором на основе никеля до ксилита. Также возможно сначала провести гидрирование смеси моносахаридов, а затем отделить образованный ксилит. Полученный ксилит очищают перекристаллизацией.
Теоретически ксилит также можно получить методом микробиологической ферментации.
Метаболизм у человека
правитьПищевая ценность ксилита составляет около 2,4 ккал/г или 10 кДж/г, но фактическое значение может варьироваться. Гликемический индекс ксилита составляет около 13 (у глюкозы — 100). У человека около 50 % ксилита всасывается из кишечника — остальное переходит в энергию кишечных бактерий, однако остальная часть выводится в неизменном виде с фекалиями. Менее 2 г из 100 г потребленного ксилита выводится с мочой. Ксилит не оказывает значительного влияния на секрецию инсулина в организме человека. Ксилит метаболизируется у людей в основном в печени, где он дегидрируется в слизистой оболочке клеток НАД- зависимой полиолдегидрогеназой (шифр КФ: 1.1.1.B19) до D-ксилулозы. Далее моносахарид фосфорилируется ксилулокиназой (шифр КФ: 2.7.1.17) до D-ксилулозо-5-фосфата, продукта пентозофосфатного пути.[3] Ксилит также образуется в организме человека в виде метаболита без внешнего потребления ксилита, оцениваемого в 2-15 г в день.
Применение
правитьВ пищевой промышленности ксилит зарегистрирован в качестве пищевой добавки E967, как подсластитель, влагоудерживающий агент, стабилизатор и эмульгатор.
Ксилит как заменитель сахара
правитьПо калорийности ксилит близок сахару (2,43 ккал/г[4] у ксилита и 3,8 ккал/г у сахара), по сладости близок к сахарозе[4], но биологической ценности не имеет. Применяется в пищевой промышленности, например вместо сахара в производстве жевательных резинок и кондитерских изделий для больных диабетом.
Применение в медицине
правитьКсилит назвали углеводосодержащим неферментируемым спиртом, дружественным зубам.[5][6] Представляется, что он обладает большим числом достоинств, чем другие многоатомные спирты[7].
Ксилит способствует образованию тромбов и увеличивает риски сердечно-сосудистых событий[8].
Слабительное действие
правитьКсилитол — слабительное средство. Взрослые хорошо переносят ксилит в суточных дозах около 40 г, но употребление взрослым более 100 г вещества в день может вызвать диарею.[9] У детей суточная доза выше 45 г также может вызвать диарею. Ксилит практически не метаболизируется в человеческом организме, поэтому в кишечник он попадает практически неизменным. Кишечные бактерии потребляют 50-75 % попавшего в организм ксилита, который далее преобразуется ими в короткоцепочечные жирные кислоты (пропионовая кислота и др.), а также в газы (водород, метан и диоксид углерода). Попадая в кишечник, ксилит также затрудняет всасывание воды стенками кишечника, что и обуславливает слабительный эффект. Данный эффект наблюдается и у некоторых других полиолов, например, у сорбита, который примерно в 2 раза сильнее оказывает слабительное действие, чем ксилит.
Токсичность для животных
правитьДля большинства млекопитающих ксилит нетоксичен, однако у собак ксилит вызывает быстрый дозозависимый выброс в кровь инсулина, дозы выше ~75-100 мг ксилита на килограмм веса приводят к гипогликемии, при дозах выше 500 мг/кг ксилит может вызывать у собак острую печеночную недостаточность, механизм такого действия в настоящее время неизвестен[10][11].
Ксилит является относительно безопасным веществом для кошек[12], лошадей, крыс и макак-резусов[11].
Ксилитан
правитьМоноангидрид ксилита C5H10O4 (1,4-ангидроксилит[13]) имеет тривиальное название «ксилитан» и применяется как заменитель глицерина в различных областях промышленности[14] (при производстве линолеума, бытовой химии и баллиститных порохов, в бумажной и текстильной промышленности и т. д.).
Примечания
править- ↑ Bradley J., Williams A., Andrew S.I.D. Lang Jean-Claude Bradley Open Melting Point Dataset // (unknown type) — 2014. — doi:10.6084/M9.FIGSHARE.1031637.V2
- ↑ Fazer ryhtyy valmistamaan ksylitolia kauran kuoresta – investoi 40 miljoonaa euroa Lahteen (фин.). Maaseudun Tulevaisuus. Дата обращения: 26 октября 2020. Архивировано 6 марта 2019 года.
- ↑ Geoffrey Livesey. Health potential of polyols as sugar replacers, with emphasis on low glycaemic properties (англ.) // Nutrition Research Reviews. — 2003-12. — Vol. 16, iss. 2. — P. 163–191. — ISSN 1475-2700 0954-4224, 1475-2700. — doi:10.1079/NRR200371.
- ↑ 1 2 МЕДИКО-ТЕХНОЛОГИЧЕСКИЕ АСПЕКТЫ ИСПОЛЬЗОВАНИЯ ЗАМЕНИТЕЛЕЙ САХАРА В МОЛОЧНЫХ ПРОДУКТАХ (недоступная ссылка) // Сборник научных трудов СевКавГТУ. Серия «Продовольствие». 2006. № 2. «Ксилит — пятиатомный спирт, … Калорийность — 3,67 ккал/г, сладость близка к сахарозе.»
- ↑ Edwardsson, Stig; Birkhed, Dowen; Mejàre, Bertil. Acid production from Lycasin, maltitol, sorbitol and xylitol by oral streptococci and lactobacilli (англ.) // Acta Odontologica Scandinavica[англ.] : journal. — 1977. — Vol. 35, no. 5. — P. 257—263. — doi:10.3109/00016357709019801. — PMID 21508.
- ↑ Drucker, D.B.; Verran, J. Comparative effects of the substance-sweeteners glucose, sorbitol, sucrose, xylitol and trichlorosucrose on lowering of pH by two oral Streptococcus mutans strains in vitro (англ.) // Archives of Oral Biology[англ.] : journal. — 1979. — Vol. 24, no. 12. — P. 965—970. — doi:10.1016/0003-9969(79)90224-3. — PMID 44996.
- ↑ Maguire, A; Rugg-Gunn, A J. Xylitol and caries prevention — is it a magic bullet? (англ.) // British Dental Journal[англ.] : journal. — 2003. — Vol. 194, no. 8. — P. 429—436. — doi:10.1038/sj.bdj.4810022. — PMID 12778091. Архивировано 28 января 2013 года.
- ↑ https://academic.oup.com/eurheartj/advance-article-abstract/doi/10.1093/eurheartj/ehae244/7683453
- ↑ Prathibha Anand Nayak, Ullal Anand Nayak, Vishal Khandelwal. The effect of xylitol on dental caries and oral flora (англ.) // Clinical, Cosmetic and Investigational Dentistry. — 2014-11. — P. 89. — ISSN 1179-1357. — doi:10.2147/CCIDE.S55761. Архивировано 31 октября 2020 года.
- ↑ Xylitol - Toxicology. Merck Veterinary Manual. Дата обращения: 26 октября 2020. Архивировано 29 октября 2020 года.
- ↑ 1 2 Renee D. Schmid, Lynn R. Hovda. Acute Hepatic Failure in a Dog after Xylitol Ingestion (англ.) // Journal of Medical Toxicology. — 2016-06. — Vol. 12, iss. 2. — P. 201–205. — ISSN 1937-6995 1556-9039, 1937-6995. — doi:10.1007/s13181-015-0531-7.
- ↑ Á. Jerzsele, Z. Karancsi, E. Pászti-Gere, Á. Sterczer, A. Bersényi. Effects of p.o. administered xylitol in cats (англ.) // Journal of Veterinary Pharmacology and Therapeutics. — 2018-06. — Vol. 41, iss. 3. — P. 409–414. — doi:10.1111/jvp.12479.
- ↑ Аникеева и др., 1976, с. 122.
- ↑ Химические товары / под ред. И. В. Лебедева. — М. : Химия, 1969. — С. 454—455. — (Справочник : в 5 т. ; т. 2).
Литература
править- Аникеева, А. Н. Ксилит и его производные / А. Н. Аникеева, Г. М. Зарубинский, С. Н. Данилов // Успехи химии. — 1976. — Т. 45, № 1. — С. 106—137.
В статье есть список источников, но не хватает сносок. |
В другом языковом разделе есть более полная статья Xylitol (англ.). |
