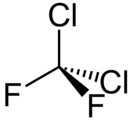
Дифтордихлормета́н (он же дихлордифтормета́н, фрео́н R 12, фрео́н-12, хладо́н-12, CFC-12, аркто́н 6, R-12) — органическое вещество, производное метана, полностью замещённый галогеналкан, фреон с формулой CCl2F2. При нормальных условиях представляет собой бесцветный негорючий газ, при высокой концентрации имеет лёгкий эфироподобный запах.
| Дифтордихлорметан | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
Дихлордифторметан | ||
| Сокращения | R-12; CFC-12; P-12; E940; HFC12 | ||
| Традиционные названия | Дифторид дихлорида углерода; Дифтордихлорметан; Фреон 12; Пропеллент 12; fluorocarbon-12, Arcton 6; Arcton 12; Фторуглерод 12; Genetron 12; Хладагент 12 | ||
| Хим. формула | |||
| Рац. формула | |||
| Физические свойства | |||
| Состояние | бесцветный газ | ||
| Молярная масса | 120,913 г/моль | ||
| Плотность | 1,486 г/см3 (жидкий, при -29,8 °C) | ||
| Энергия ионизации | 11,75 ± 0,01 эВ[5][6] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -155,95 [1] | ||
| • кипения | 243,24 К; -29,74[1] °C | ||
| Критическая точка | |||
| • температура | 112[2] °C | ||
| • давление | 4,119 МПа[2] | ||
| Критическая плотность | 579,1 кг/м3 см³/моль | ||
| Энтальпия | |||
| • кипения | 20,01 кДж/моль | ||
| Давление пара | 5,7 ± 0,1 атм[5] | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | 0,286 г/л при 20 °C | ||
| • в в органических растворителях | растворим | ||
| Структура | |||
| Дипольный момент | 1,7E−30 Кл·м[6] | ||
| Классификация | |||
| Рег. номер CAS | 75-71-8 | ||
| PubChem | 6391 | ||
| Рег. номер EINECS | 200-893-9 | ||
| SMILES | |||
| InChI | |||
| Кодекс Алиментариус | E940 | ||
| RTECS | PA8200000 | ||
| ChEBI | 229860 | ||
| Номер ООН | 1028 | ||
| ChemSpider | 6151 | ||
| Безопасность | |||
| Предельная концентрация | 3000 мг/м³ | ||
| ЛД50 | 12000 - 36000 мг/кг[3][4] | ||
| Токсичность | Зарегистрированные препараты дифтордихлорметана относятся к 4-му классу опасности для человека. | ||
| Сигнальное слово | Осторожно | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Является сильным разрушающим озоновый слой в атмосфере Земли агентом, в связи с чем его производство и использование в 1989 году было запрещено в развитых странах (странах, не подпадающих под действие статьи 5 Монреальского протокола)[7].
Получение
правитьПолучают взаимодействием четыреххлористого углерода с фтороводородом в присутствии пентахлорида сурьмы в качестве катализатора[8]:
- .
Побочными продуктами этой реакции являются трихлорфторметан ( ), хлортрифторметан ( ) и тетрафторметан ( ).
Физические свойства
правитьПри нормальных условиях представляет собой тяжёлый, примерно в 4 раза тяжелее воздуха, бесцветный газ, со слабым эфирным запахом.
Ниже −29,8 °C при атмосферном давлении сжижается в бесцветную жидкость.
Растворяется в большинстве органических растворителей.
Применение
правитьИспользовался как холодильный агент и в качестве пропеллента в аэрозольных баллонах, в настоящее время его применение запрещено Монреальским протоколом.
Влияние на экологию
правитьДифтордихлорметан обладает высокой озоноразрушающей активностью, образуя озоновые дыры. Поэтому его производство и использование ограничено Монреальским протоколом. К 1994 году был в основном заменён тетрафторэтаном.
Коэффициент возможности истощения озонового слоя (ODP) 0,9 (CCl3F = 1). Потенциал глобального потепления (GWP) 8500 (CO2 = 1)[1].
-
Рост концентрации CFC-12 в атмосфере
-
Карта концентраций CFC-12 на уровне моря, 1990 год
-
Карта концентраций CFC-12 над океаном, 1990 год
-
Вертикальные профили концентраций CFC-12, CFC-11, H-1211 и SF6
Опасность для здоровья
правитьОказывает раздражающее действие на органы дыхания, снижает сократительную способность миокарда, артериальное давление, нарушает сердечную проводимость, повышает сопротивление лёгочных сосудов, угнетает центральную нервную систему.
Острые отравления обычно связаны как с действием самого вещества, так и продуктов его разложения (при термическом разложении при нагревании выше 150 °C образуется фосген, в присутствии кислорода разлагается с выделением хлороводородной и фтороводородной кислот, карбонилгалогенидов).
При лёгких отравлениях пострадавшие жалуются на головную боль, головокружения, слабость, тошноту, рвоту, иногда повышенную сонливость. Это состояние длится от нескольких часов до 1—2 суток. В более тяжёлых случаях возможны жалобы на раздражение слизистых глаз и верхних дыхательных путей, сухость в носоглотке, ощущение удушья, тремор рук и ног, обморочное состояние, слуховые галлюцинации.
Ингаляционное воздействие приводит к раздражению слизистых поверхностей глаз и верхних дыхательных путей. При попадании на кожу возникают ожоги.
Хронические, подострые и острые отравления наносят необратимый вред здоровью.
Контакт с некоторыми химически активными металлами может привести к взрыву при определённых условиях. (например, при повышенные температуры и/или давления).
Примечания
править- ↑ 1 2 3 Фреон 12. Дата обращения: 21 февраля 2021. Архивировано 24 октября 2018 года.
- ↑ 1 2 Физические свойства холодильных агентов по ГОСТ Р 12.2.142-99. Дата обращения: 21 февраля 2021. Архивировано 3 марта 2021 года.
- ↑ name=https://www.safework.ru_Freon-12 (недоступная ссылка)
- ↑ name=https://docs.cntd.ru_Дифтордихлорметан (недоступная ссылка)
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0192.html
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 1:Update on Ozone-Depleting Substances (ODSs) and Other Gases of Interest to the Montreal Protocol // Scientific assessment of ozone depletion: 2018.. — Global Ozone Research and Monitoring Project–Report No. 58. — Geneva, Switzerland : World Meteorological Organization, 2018. — P. 1.10. — ISBN 978-1-7329317-1-8. Архивная копия от 5 марта 2021 на Wayback Machine Источник. Дата обращения: 21 февраля 2021. Архивировано 5 марта 2021 года.
- ↑ Гринвуд Н. Н., Эрншоу А. Химия элементов в 2-х т. — М.: Бином. Лаборатория знаний, 2015.
См. также
правитьВ статье не хватает ссылок на источники (см. рекомендации по поиску). |