Артемизинин
Артемизинин и его полусинтетические производные — это группа препаратов, которые обладают наиболее быстрым действием среди всех существующих в настоящее время лекарств против тропической малярии, вызванной паразитом Plasmodium falciparum[1]. Этот препарат был открыт в 1972 году китайским фармакологом Ту Юю, получившей за это открытие в 2015 году половину Нобелевской премии по медицине и физиологии[2][3]. Использование лекарств, содержащих производные артемизинина (артемизинин-комбинированные препараты), в настоящее время является стандартом лечения тропической малярии во всем мире. Артемизинин выделяют из полыни однолетней (Artemisia annua), используемой в традиционной китайской медицине. Соединение-предшественник может быть получено с использованием генетически модифицированных дрожжей.
| Артемизинин | |
|---|---|
| Artemisinin | |
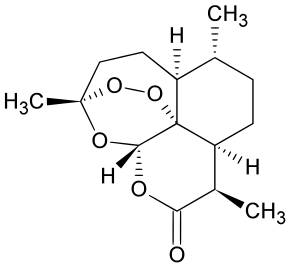 | |
| Химическое соединение | |
| ИЮПАК | (3''R'',5a''S'',6''R'',8a''S'',9''R'',12''S'',12a''R'')-октагидро-3,6,9-триметил-3,12-эпокси-12''H''-пирано[4,3-''j'']-1,2-бензодиоксипин-10(3''H'')-1 |
| Брутто-формула | C15H22O5 |
| Молярная масса | 282.332 г/моль |
| CAS | 63968-64-9 |
| PubChem | 68827 |
| DrugBank | DB13132 |
| Состав | |
| Классификация | |
| АТХ | P01BE01 |
| Фармакокинетика | |
| Биодоступн. | высокая |
| Лекарственные формы | |
| порошок для приготовления инъекционного раствора для в/в введении | |
| Способы введения | |
| внутривенно | |
История открытия
правитьТу Юю открыла артемизинин, работая в рамках китайского секретного Проекта 523, нацеленного на поиск лекарства от малярии для помощи северным вьетнамцам во главе с Хо Ши Мином во время войны во Вьетнаме. Ту Юю работала в Академии народной медицины и поэтому сконцентрировалась на поиске и проверке народных средств борьбы с малярией. Коллектив под её руководством проанализировал около 2000 рецептов, на основе 640 выбранных из них предписаний они изготовили 380 экстрактов, которые проверяли на животных[3]. Так в 1971 году был найден один из них, артемизинин, имеющий хорошие противомалярийные показатели. Он изготавливался из полыни однолетней (Artemisia annua) по рецепту из третьей части книги Гэ Хуна «Чжоухоу бэйцзифан» («Предписания для неотложной помощи»), относящейся к 340 году н. э.[4][5] В 1973 году группа Ту Юю синтезировала производные: артеметер, артесунат и дигидроартемизинин, который, как оказалось позднее, был более эффективен, чем артемизинин в его первоначальном виде[6].
Описание
правитьС точки зрения химии артемизинин — это сесквитерпеновый лактон, содержащий необычный пероксидный мостик. Этот пероксидный мостик считается ответственным за механизм действия препарата. Известно очень немного других природных соединений с таким пероксидным мостиком[7]. Наиболее известные производные артемизинина, обладающие ещё большей активностью, чем исходный артемизинин — это дигидроартемизинин, артеметер (жирорастворимый метиловый эфир артемизинина) и артесунат (водорастворимый гемисукцинат дигидроартемизинина).
Артемизинин и его эндопероксидные производные используются для лечения малярии, но их низкая биологическая усваиваемость, плохие фармакокинетические характеристики и высокая стоимость препаратов стали основными препятствиями для их использования в качестве монотерапии. Использование препарата в качестве монотерапии не одобряется Всемирной организации здравоохранения, поскольку есть признаки того, что у малярийных паразитов развивается устойчивость к этому препарату. Применение артемизинина или его производных в комбинации с другими противомалярийными препаратами является намного более предпочтительным методом лечения малярии, поскольку оно более эффективно и легче переносится пациентами. Препарат все чаще используется и при лечении трехдневной малярии, вызванной паразитом Plasmodium vivax[8]. Также ведутся исследования по использованию этого препарата для лечения рака.
Неосложнённая малярия
правитьАртемизинины могут быть использованы в качестве монотерапии, но это приводит к высокой вероятности рецидива заболевания, и для того чтобы очистить организм от всех паразитов и не допустить повторения заболевания, необходимы другие препараты. Всемирная организация здравоохранения (ВОЗ) оказывает давление на производителей лекарств, запрещая им выпускать некомбинированные препараты артемизинина для широкого потребления, понимая, что если у малярийного паразита разовьётся устойчивость к артемизинину и его производным, то это приведёт к катастрофе[9].
ВОЗ рекомендует использовать комбинированные c артемизинином препараты в качестве приоритетной терапии при лечении тропической малярии во всём мире[10]. Комбинации препаратов являются более эффективными, потому что их компонент артемизинин убивает большинство паразитов в начале лечения, в то время как второй, более медленно выводящийся из организма компонент препарата убивает оставшихся паразитов[11].
В настоящий момент доступны несколько лекарственных препаратов, содержащих в себе кроме артемизинина и второй компонент, который имеет длительный период полувыведения, например мефлохин, люмефантрин, амодиахин, пиперахин и пиронаридин[12]. Все чаще эти комбинации делаются с использованием стандарта GMP ввиду зачастую низкого качества некоторых продающихся в Африке и Юго-Восточной Азии артемизинин-содержащих препаратов[13][14].
Осложнённая малярия
правитьАртесунат, введённый внутривенно или внутримышечно, показал себя более эффективным, чем хинин в больших, случайных, контролируемых испытаниях как у взрослых[15], так и у детей[16]. В результате этих испытаний выяснилось, что применение артесуната снижает смертность примерно на 30 % по сравнению с хинином. Причины этого различия заключаются в меньшем количестве случаев гипогликемии, более лёгком введении препарата и более быстром действии как против циркулирующих, так и изолированных паразитов. На данный момент артесунат рекомендован ВОЗ для лечения всех случаев осложнённой малярии. Эффективное лечение с применением артемизинин-комбинированных препаратов привело к снижению заболеваемости и смертности от малярии в течение двух лет примерно на 70 %[17].
Лечение рака
правитьАртемизинин проходит испытания в качестве лекарства для лечения рака[18]. Артемизинин показал противоопухолевый эффект в экспериментальных моделях на гепатоцеллюлярной карциноме[19] . Он имеет пероксидно-лактонную группу в своей структуре, и считается, что, когда пероксид вступает в контакт с высокими концентрациями железа (которые часто встречаются в раковых клетках), молекула становится нестабильной и образуются активные формы кислорода. Было показано, что происходит снижение ангиогенеза и экспрессия фактора роста эндотелия сосудов в некоторых культурах тканей. Последние фармакологические данные свидетельствуют о том, что дигидроартемизинин (производное артемизинина) способен поражать метастатические клетки меланомы человека в пробирке, вызывая митохондриальный апоптоз, что приводит к снижению железо-зависимой генерации цитотоксического окислительного стресса[20]. Экспериментальные исследования по использованию артесуната (производное артемизинина) дали многообещающие результаты для лечения колоректального рака[21].
Паразитические гельминты
правитьВ поисках новых противогельминтных средств для лечения шистосомоза в Китае было сделано открытие, связанное с тем, что артемизинин эффективен против шистосом, человеческих кровяных сосальщиков, которые являются второй наиболее распространённой паразитарной инфекцией после малярии. Артемизинин и все его производные эффективно действует на гельминтов[22]. Позже было обнаружено, что артемизинины обладают широким спектром активности против многих видов трематод, в том числе Schistosoma japonicum, Schistosoma mansoni, Schistosoma haematobium, Clonorchis sinensis, Fasciola hepatica и Opisthorchis viverrini[23]. В Кот-д’Ивуаре[24] и Китае[25] были успешно проведены клинические испытания артемизинина на пациентах с шистосомозом.
Побочные действия
правитьАртемизинины, как правило, хорошо переносятся в дозах, используемых для лечения малярии[26]. Побочные эффекты от препаратов артемизининового класса схожи с симптомами малярии: тошнота, рвота, анорексия, головокружение и лёгкие нарушения крови[26][27]. Редким, но серьёзным побочным эффектом является аллергическая реакция. Уже сообщалось об одном случае значительного воспаления печени в связи с длительным использованием относительно высоких доз артемизинина.[28].
Устойчивость к артемизинину
правитьКлинические данные относительно устойчивости к артемизинину впервые появились в 2008[29] году в юго-восточной Азии. Впоследствии они были подтверждены после детального изучения в западной Камбодже. В 2012 году сообщалось об устойчивости к артемизинину в соседнем Таиланде, а в 2014 году такие же данные появились в Камбодже, Вьетнаме, Лаосе, Мьянме и в юго-восточной Азии[30][31].
Механизм действия
правитьБольшинство используемых сегодня артемизининов являются химически модифицированными формами биологически активного метаболита дигидроартемизинина, который является активным на стадии, когда паразит находится внутри красных кровяных клеток. Артемизинин оказывают своё действие на паразитов посредством образования свободных радикалов, за счёт наличия у артемизининов эндопероксидного мостика. Когда паразит, который вызывает малярию, заражает эритроцит, он потребляет гемоглобин в пределах своей пищеварительной вакуоли, и этот процесс вызывает оксидативный стресс. В первоначальной теории механизма действия железо непосредственно восстанавливает пероксидную связь артемизинина, генерируя высоко валентные виды оксида железа и в результате происходит целый каскад реакций, которые производят реактивные кислородные радикалы, повреждающие паразитов и приводящие к их смерти. Однако после широкого обсуждения этого механизма появились и другие гипотезы. Одним из вариантов является то, что артемизинин нарушает клеточные окислительно-восстановительные процессы. Артесунат эффективно ингибирует важный для паразита белок — мембранную глутатион S-трансферазу. Недавно был предложен свободно-радикальный механизм, в котором артемизинин активируется вследствие наличия железа в пищевой вакуоли, который, в свою очередь ингибирует кальциевый АТФ-фермент PfATP6 путём прекращения фосфорилирования и нуклеотидного связывания, приводя к потере функции АТФ-фермента PfATP6 паразита и его гибели.
Дозировка
правитьПроизводные артемизинина имеют период полувыведения порядка одного часа. Таким образом, они требуют по крайней мере многократного ежедневного введения препарата в течение нескольких дней. Например, одобренная ВОЗ доза для взрослых составляет по четыре таблетки артемизин-люмефантрина каждые 12 часов[32][33].
Синтез
правитьБиосинтез в полыни однолетней
правитьБиосинтез артемизинина в полыни однолетней (Artemisia annua) вероятнее всего происходит в две стадии: через биосинтез холестерина (мевалонатный путь) и циклизацию промежуточного метаболита — фарнезилдифосфата. Также возможен и немевалонатный путь биосинтеза артемизинина, в котором происходит образование пятиуглеродных молекул-предшественников, таких как изопентенилпирофосфат и диметилаллилпирофосфат, как это происходит в других системах биосинтеза сесквитерпенов. Пути, по которым происходит превращение артемизининола в артемизинин, остаются спорными. Они отличаются друг от друга в основном тем, когда именно происходит стадия восстановления. Но в каждом из них дигидроартемизининовая кислота выступает в качестве окончательного предшественника артемизинина. Дигидроартемизининовая кислота путём фото-окисления превращается в гидропероксид дигидроартемизининовой кислоты. Завершает процесс биосинтеза артемизинина расширение кольца через разрыв гидропероксида и второе окисление до пероксида с участием кислорода.
Примечания
править- ↑ White N.J. Assessment of the pharmacodynamic properties of antimalarial drugs in vivo (англ.) // Antimicrob. Agents Chemother.[англ.] : journal. — 1997. — July (vol. 41, no. 7). — P. 1413—1422. — PMID 9210658. — PMC 163932.
- ↑ The Nobel Prize in Physiology or Medicine 2015 (PDF). Nobel Foundation. Дата обращения: 7 октября 2015. Архивировано 6 января 2019 года.
- ↑ 1 2 Кирилл Стасевич. Китайская народная медицина и почвенные бактерии против малярии и слоновой болезни // Наука и жизнь. — 2015. — № 11. — С. 2—7. Архивировано 28 июля 2017 года.
- ↑ Е. Клещенко. Победители паразитов // Химия и жизнь. — 2015. — № 11. Архивировано 6 января 2016 года.
- ↑ Имеется в виду следующая цитата из этой книги: кит. 又方 青蒿一握。以水二升漬,絞取汁。盡服之。, англ. Ge Hong. Zhou hou bei ji fang [Emergency Prescriptions kept up one’s Sleeve] Jin, 4th c. (340 AD)., перевод рецепта на английский по статье Hsu, 2006: «Another recipe: qinghao, one bunch, take two sheng[2 × 0.2 l] of water for soaking it, wring it out, take the juice, ingest it in its entirety.»
- ↑ Hsu, 2006.
- ↑ Geoff Brown. Artemisinin and a new generation of antimalarial drugs (англ.). Education in Chemistry. Royal Society of Chemistry (1 июня 2006). Дата обращения: 26 декабря 2015. Архивировано из оригинала 6 октября 2015 года.
- ↑ Douglas N.M., Anstey N.M., Angus B.J., Nosten F., Price R.N. Artemisinin combination therapy for vivax malaria (англ.) // The Lancet : journal. — Elsevier, 2010. — June (vol. 10, no. 6). — P. 405—416. — doi:10.1016/S1473-3099(10)70079-7. — PMID 20510281. — PMC 3350863.
- ↑ Rehwagen C. WHO ultimatum on artemisinin monotherapy is showing results (англ.) // BMJ : journal. — 2006. — May (vol. 332, no. 7551). — P. 1176. — doi:10.1136/bmj.332.7551.1176-b. — PMID 16709988. — PMC 1463909.
- ↑ Guidelines for the Treatment of Malaria : [англ.] : [арх. 9 июля 2021]. — 3rd ed. — Geneva : World Health Organization, 2015. — 313[2] p. — ISBN 978-92-4-154912-7.
- ↑ White, N. J. Antimalarial drug resistance : [англ.] // Journal of Clinical Investigation. — 2004. — Vol. 113, no. 8 (April). — P. 1084—1092. — doi:10.1172/JCI21682. — PMID 15085184. — PMC 385418.
- ↑ Krudsood S., Looareesuwan S., Tangpukdee N. et al. New Fixed-Dose Artesunate-Mefloquine Formulation against Multidrug-Resistant Plasmodium falciparum in Adults: a Comparative Phase IIb Safety and Pharmacokinetic Study with Standard-Dose Nonfixed Artesunate plus Mefloquine (англ.) // Antimicrob Agents Chemother[англ.] : journal. — 2010. — June (vol. 54, no. 9). — P. 3730—3737. — doi:10.1128/AAC.01187-09. — PMID 20547795. — PMC 2935027.
- ↑ "Malaria drugs recalled in Kenya". BBC News. 2007-08-17. Архивировано 5 марта 2016. Дата обращения: 26 декабря 2015.
- ↑ Newton P., Proux S., Green M. et al. Fake artesunate in southeast Asia (англ.) // The Lancet. — Elsevier, 2001. — June (vol. 357, no. 9272). — P. 1948—1950. — doi:10.1016/S0140-6736(00)05085-6. — PMID 11425421.
- ↑ Dondorp A., Nosten F., Stepniewska K., Day N., White N. Artesunate versus quinine for treatment of severe falciparum malaria: a randomised trial (англ.) // The Lancet : journal. — Elsevier, 2005. — Vol. 366, no. 9487. — P. 717—725. — doi:10.1016/S0140-6736(05)67176-0. — PMID 16125588.
- ↑ Dondorp A.M., Fanello C.I., Hendriksen I.C. et al. Artesunate versus quinine in the treatment of severe falciparum malaria in African children (AQUAMAT): an open-label, randomised trial (англ.) // The Lancet : journal. — Elsevier, 2010. — November (vol. 376, no. 9753). — P. 1647—1657. — doi:10.1016/S0140-6736(10)61924-1. — PMID 21062666. — PMC 3033534.
- ↑ Bhattarai, Achuyt; Ali, Abdullah S; Kachur, S. Patrick; Mårtensson, Andreas; Abbas, Ali K; Khatib, Rashid; Al-mafazy, Abdul-wahiyd; Ramsan, Mahdi; Rotllant, Guida. Impact of Artemisinin-Based Combination Therapy and Insecticide-Treated Nets on Malaria Burden in Zanzibar (англ.) // PLoS Med[англ.] : journal. — 2007. — 6 November (vol. 4, no. 11). — P. e309. — doi:10.1371/journal.pmed.0040309. — PMID 17988171. — PMC 2062481.
- ↑ University of Washington: Artemisinin Архивная копия от 26 октября 2008 на Wayback Machine Lai H, Singh NP, Sasaki T. (2013) Development of artemisinin compounds for cancer treatment. Invest New Drugs 31:230–246.
- ↑ Hou J., Wang D., Zhang R., Wang H. Experimental therapy of hepatoma with artemisinin and its derivatives: in vitro and in vivo activity, chemosensitization, and mechanisms of action (англ.) // Clin Cancer Res[англ.] : journal. — 2008. — Vol. 14, no. 7. — P. 5519—5530. — doi:10.1158/1078-0432.CCR-08-0197. — PMID 18765544.
- ↑ Cabello C.M., Lamore S.D., Bair WB 3rd, Qiao S., Azimian S., Lesson J.L., Wondrak G.T. The redox antimalarial dihydroartemisinin targets human metastatic melanoma cells but not primary melanocytes with induction of NOXA-dependent apoptosis (англ.) // Invest. New Drugs : journal. — 2011. — Vol. 30, no. 4. — P. 1289—1301. — doi:10.1007/s10637-011-9676-7. — PMID 21547369. — PMC 3203350.
- ↑ Krishna Sanjeev, Ganapathi Senthil, Ster Irina Chis, Saeed Mohamed, E.M. Cowan Matt, Finlayson Caroline, Kovacsevics Hajnalka, Jansen Herwig, Kremsner Peter G. Efferth Thomas, Kumar Devinder. A Randomised, Double Blind, Placebo-Controlled Pilot Study of Oral Artesunate Therapy for Colorectal Cancer (англ.) // EBioMedicine[англ.] : journal. — 2014. — November (vol. 2). — P. 82—90. — doi:10.1016/j.ebiom.2014.11.010.
- ↑ Xiao SH. Development of antischistosomal drugs in China, with particular consideration to praziquantel and the artemisinins (англ.) // Acta Trop. : journal. — 2005. — Vol. 96, no. 2—3. — P. 153—167. — doi:10.1016/j.actatropica.2005.07.010. — PMID 16112072.
- ↑ Keiser J., Utzinger J. Artemisinins and synthetic trioxolanes in the treatment of helminth infections (англ.) // Current Opinion in Infectious Diseases : journal. — Lippincott Williams & Wilkins[англ.], 2007. — Vol. 20, no. 6. — P. 605—612. — doi:10.1097/QCO.0b013e3282f19ec4. — PMID 17975411.
- ↑ Utzinger J., N'Goran E.K., N'Dri A., Lengeler C., Xiao S., Tanner M. Oral artemether for prevention of Schistosoma mansoni infection: randomised controlled trial (англ.) // The Lancet : journal. — Elsevier, 2000. — Vol. 355, no. 9212. — P. 1320—1325. — doi:10.1016/S0140-6736(00)02114-0. — PMID 10776745. Архивировано 4 мая 2018 года.
- ↑ Li Y.S., Chen H.G., He H.B., Hou X.Y., Ellis M., McManus DP. A double-blind field trial on the effects of artemether on Schistosoma japonicum infection in a highly endemic focus in southern China (англ.) // Acta Trop. : journal. — 2005. — Vol. 96, no. 23. — P. 184—190. — doi:10.1016/j.actatropica.2005.07.013. — PMID 16112071.
- ↑ 1 2 Taylor W.R., White N.J. Antimalarial drug toxicity: a review (англ.) // Drug Saf[англ.] : journal. — 2004. — Vol. 27, no. 1. — P. 25—61. — doi:10.2165/00002018-200427010-00003. — PMID 14720085.
- ↑ Leonardi E., Gilvary G., White N.J., Nosten F. Severe allergic reactions to oral artesunate: a report of two cases (англ.) // Trans. R. Soc. Trop. Med. Hyg.[англ.] : journal. — 2001. — Vol. 95, no. 2. — P. 182—183. — doi:10.1016/S0035-9203(01)90157-9. — PMID 11355556.
- ↑ Hepatitis Temporally Associated with an Herbal Supplement Containing Artemisinin — Washington, 2008. CDC. Дата обращения: 3 октября 2017. Архивировано 27 августа 2017 года.
- ↑ Noedl, H; Se, Y; Schaecher, K; Smith, B. L.; Socheat, D; Fukuda,. Evidence of artemisinin-resistant malaria in western Cambodia (англ.) // New England Journal of Medicine : journal. — 2008. — Vol. 359, no. 24. — P. 2619—2620. — doi:10.1056/NEJMc0805011. — PMID 19064625.
- ↑ Briggs, Helen (30 July 2014) Call for 'radical action' on drug-resistant malaria Архивная копия от 31 июля 2014 на Wayback Machine BBC News, health, Retrieved 30 July 2013
- ↑ Ashley Elizabeth A. Dhorda Mehul et al. Spread of Artemisinin Resistance in Plasmodium falciparum Malaria (англ.) // The New England Journal of Medicine : journal. — 2014. — 31 July (vol. 371, no. 5). — P. 411—423. — doi:10.1056/NEJMoa1314981. — PMID 25075834. Архивировано 5 сентября 2015 года.
- ↑ Vugt M.V., Wilairatana P., Gemperli B. et al. Efficacy of six doses of artemether-lumefantrine (benflumetol) in multidrug-resistant Plasmodium falciparum malaria (англ.) // Am J Trop Med Hyg[англ.] : journal. — 1999. — Vol. 60, no. 6. — P. 936—942. — PMID 10403324.
- ↑ Lefevre G., Looareesuwan S., Treeprasertsuk S. et al. A clinical and pharmacokinetic trial of six doses of artemether-lumefantrine for multidrug-resistant Plasmodium falciparum malaria in Thailand (англ.) // Am J Trop Med Hyg[англ.] : journal. — 2001. — Vol. 64, no. 5—6. — P. 247—256. — PMID 11463111.
Литература
правитьСсылки
править- History, Aetiology, Pathophysiology, Clinical Features, Diagnosis, Treatment, Complications And Control Of Malaria: Artemisinin Derivatives
- Design and synthesis of antimalarial endoperoxides
- https://gmpnews.ru/2020/03/v-biotexnoparke-kolcovo-budet-sozdano-proizvodstvo-artemizinina-i-artemizininovoj-kisloty/
- van Vugt M., Looareesuwan S., Wilairatana P. et al. Artemether-lumefantrine for the treatment of multidrug-resistant falciparum malaria (англ.) // Trans. R. Soc. Trop. Med. Hyg.[англ.] : journal. — 2000. — Vol. 94, no. 5. — P. 545—548. — doi:10.1016/S0035-9203(00)90082-8. — PMID 11132386.
- Daviss B. Malaria, Science, and Social Responsibility: Nonprofit drug-development partnership seeks to cure the ills of developing nations (англ.) // The Scientist : journal. — 2005. — Vol. 19, no. 6. — P. 42.
- Research on the use of artemisinin for cancer treatment
- Artemisinin — Researchers blend folk treatment, high tech for promising anti-cancer compound
- BBC Horizon documentary about artemisinin
- Artemisia Annua, by Memorial-Sloan Kettering Cancer Center
- Use of Artemisinin for Cancer Treatment and Bacterial Infection, Henry Lai, Ph.D., University of Washington (streaming video, Spring 2005)
- Assured Artemisinin Supply System, support the global production of sufficient Artemisia/artemisinin to meet the expanded needs
- Artemisinin latest patents, covering use in fighting infections, including viral infections; fighting cancer; various novel derivatives and ACTs; high-yielding Artemisia plants; and extraction methods.