Ксантон
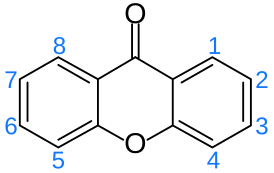
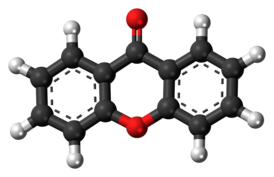
Ксантон (также окись дифениленкетона, дибензо-γ-пирон) — органическое соединение с химической формулой C13H8O2. Получают при нагреве фенил-салицилата[1]. В 1939 году ксантон начали использовать в качестве инсектицида[2]. Ксантон используют также для получения ксантгидрола, применяемого для контроля уровня мочевины в крови.
| Ксантон | |
|---|---|
  | |
| Общие | |
| Систематическое наименование |
9H-xanthen-9-one |
| Традиционные названия | ксантон, xanthone, окись дифениленкетона, дибензо-γ-пирон |
| Хим. формула | C13H8O2 |
| Физические свойства | |
| Молярная масса | 196,19 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 174 °C |
| • кипения | 351 °C |
| Классификация | |
| Рег. номер CAS | 90-47-1 |
| PubChem | 7020 |
| Рег. номер EINECS | 201-997-7 |
| SMILES | |
| InChI | |
| ChEBI | 37647 |
| ChemSpider | 6753 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
В конце XIX века использовался как сырьё для синтетических органических красок жёлтого оттенка.
В природе
правитьХимическая структура ксантона является основой различных естественных органических соединений, которые иногда вместе именуются ксантонами. Чаще всего их связывают с тропическим фруктом мангостан, в кожуре которого содержится более 40 подобных соединений.[3]
Известно около 200 ксантонов. Ксантоны являются естественными составляющими растений в семействах Боннетовые (Bonnetiaceae) и Клузиевые (Clusiaceae), можно найти в некоторых видах в семействе Подостемовые (Podostemaceae) (все эти семейства относятся к одному порядку — Мальпигиецветные)[4].
Ксантоны
правитьКсантоны - класс природных фенольных соединений, имеющих структуру дибензо-у-пирона. Название ксантонов происходит от греческого xanthos, что значит желтый, так как природные производные ксантона имеют желтую или кремовую окраску. Углубленные исследования ксантонов начались с 1969 г. в Японии, Франции, США, Швеции, Индии, а также в странах СНГ. В настоящее время насчитывается до 300 ксантоновых производных, выделенных из растений. Среди большого числа известных ксантонов особенно широко распространены С-гликозиды мангиферин и изомангиферин. Они плохо растворимы в воде, растворимы в спирте, ацетоне, этилацетате, нерастворимы в хлороформе, дихлорэтане.
Получение
правитьРеакции
правитьПри осторожном сплавлении с едким кали ксантон превращается в диоксибензофенон. При обработке цинковой пылью, соляной кислотой и кристаллической уксусной кислотой ксантон переходит (аналогично бензофенону) — в двуокись этилен-тетрафенилена: O(C 6H4)2C:C(C6H4)2 O (темп. плавл. 315°). Подобно флавонам, ксантон не реагирует с гидроксиламином и фенилгидразином (оксим и гидразон ксантона). Впрочем, они получены Гребе и Редером (1899) через посредство ксантиона. О(C 6H4)2 CS (темп. плавл. 156°), полученного действием H 2 S на ксантоанил, О(C 6H4)2 С:N.С 6 Н 5 (темп. плавл. 134°).
Физические свойства
правитьКсантон кристаллизуется в жёлтых иглах и является хромогенным веществом. Очень устойчив к ультрафиолетовому излучению. Может использоваться в солнечных батареях.
Примечания
править- ↑ Organic Syntheses, Coll. Vol. 1, p.552 (1941) — preparation of xanthone
- ↑ Steiner, L. F. and S. A. Summerland.. Xanthone as an ovicide and larvicide for the codling moth. // Journal of economic entomology. — 1943. — № 36. — P. 435—439.
- ↑ PubMed.gov — journal articles on xanthones
- ↑ Angiosperm Phylogeny Group (2003). An update of the Angiosperm Phylogeny Group classification for the orders and families of flowering plants: APG II. Botanical Journal of the Linnean Society 141: 399—436 (Available online: [www.blackwell-synergy.com/links/doi/10.1046/j.1095-8339.2003.t01-1-00158.x/abstract Abstract] (недоступная ссылка) | [www.blackwell-synergy.com/links/doi/10.1046/j.1095-8339.2003.t01-1-00158.x/full/ Full text (HTML)] Источник. Дата обращения: 21 ноября 2009. Архивировано из оригинала 22 декабря 2007 года. | [www.blackwell-synergy.com/links/doi/10.1046/j.1095-8339.2003.t01-1-00158.x/pdf Full text (PDF)] Источник. Дата обращения: 21 ноября 2009. Архивировано из оригинала 12 сентября 2019 года.)
Литература
править- Григорович П. С. Ксантон // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
Это заготовка статьи об органическом веществе. Помогите Википедии, дополнив её. |
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист |