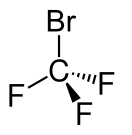
Бромтрифтормета́н (также известный как галон 1301) — органическое соединение с формулой CBrF3, производное метана, полностью замещённый галогеналкан. При нормальных условиях — негорючий прозрачный газ.
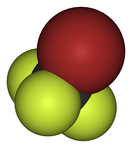
| Трифторбромметан | |||
|---|---|---|---|
 | |||
| Общие | |||
| Систематическое наименование |
Трифторбромметан | ||
| Хим. формула | CBrF3 | ||
| Физические свойства | |||
| Состояние | газообразный | ||
| Молярная масса | 148,909 г/моль | ||
| Плотность | 6,77 г/см³ | ||
| Энергия ионизации | 11,78 ± 0,01 эВ[1] и 11,4 эВ[2] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −168 °C | ||
| • кипения | −58 °C | ||
| Давление пара | 1 ± 1 атм[1] | ||
| Структура | |||
| Дипольный момент | 2,2E−30 Кл·м[2] | ||
| Классификация | |||
| Рег. номер CAS | 75-63-8 | ||
| PubChem | 6384 | ||
| Рег. номер EINECS | 200-887-6 | ||
| SMILES | |||
| InChI | |||
| RTECS | PA5425000 | ||
| Номер ООН | 1009 | ||
| ChemSpider | 6144 | ||
| Безопасность | |||
| Пиктограммы СГС |
|
||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Производство
правитьБромтрифторметан может быть получен путём взаимодействия трифторметана с бромом.
Таблица физических свойств
править| свойства | значения |
|---|---|
| Критическая температура(Тс) | 66,9 °C (340,08 K) |
| Критическое давление(pc) | 3,956 МПа (39,56 бар) |
| Критическая плотность(ρc) | 5,13 моль/л |
| Потенциал истощения озонового слоя (ODP) | 10 (CCl3F = 1) |
| Потенциал глобального потепления (GWP) | 6900 (CO2 = 1) |
Использование
правитьБромтрифторметан был введён в качестве средства пожаротушения в 1960-х годах. Бромтрифторметан тушит пожары в концентрации 6 %, вмешиваясь в радикальную реакцию горения. Относится к группе галогенированных углеводородов, вредных для озонового слоя и запрещённых Монреальским протоколом. Их производство в промышленно развитых странах (в частности, в Европейском Союзе) запрещено. Тем не менее, применение в соответствии с международным правом по-прежнему разрешено.
- Химический реагент
Бромтрифторметан является прекурсором трифторметилтриметилсилана, популярного трифторметилирующего реагента в органическом синтезе.
Токсикология и безопасность
правитьТрифторбромметан разлагается при контакте с горячей поверхностью или с пламенем, образуя токсичные пары, включая бромистый водород и фтористый водород (продукты пиролиза). Бромтрифторметан очень агрессивно реагирует со щелочными металлами.
Вещество раздражает глаза. Быстрое испарение жидкости может вызвать обморожение. Пары могут оказывать влияние на центральную нервную систему.
Литература
правитьПримечания
править- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0634.html
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5